
一定温度下,向密闭容器中充入1.0 mol N2和3.0 mol H2,反应达到平衡时,测得NH3的物质的量为0.6 mol。若该容器中开始时N2的物质的量为2.0 mol,H2为6.0 mol,则平衡时NH3的物质的量为( )
A.若为定容容器,n(NH3)=1.2 mol
B.若为定容容器,n(NH3)<1.2 mol
C.若为定压容器,n(N H3)=1.2 mol
H3)=1.2 mol
D.若为定压容器,n(NH3)>1.2 mol
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
Ⅰ.锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌。某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示: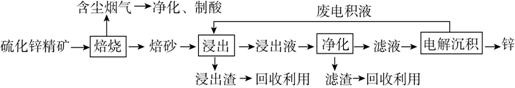
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为____________________。
(2)浸出液“净化”过程中加入的主要物质为________,其作用是________。
(3)电解沉积过程中的阴极采用铝板,阳极采用Pb-Ag合金惰性电极,阳极逸出的气体是________。
(4)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质。“氧压酸浸”中发生主要反应的离子方程式为___________________________________________。
(5)我国古代曾采用“火法”工艺冶炼锌。明代宋应星著的《天工开物》中有关于“升炼倭铅”的记载:“炉甘石十斤,装载入一泥罐内,……,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,……,冷淀,毁罐取出,……,即倭铅也。” 该炼锌工艺过程主要反应的化学方程式为_________________________________________________。(注:炉甘石的主要成分为碳酸锌,倭铅是指金属锌)
Ⅱ.工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:
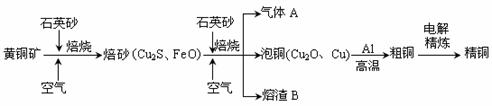
(6) 焙砂含Cu量为20%~50%。转炉中,将焙砂加熔剂(石英砂)在1200℃左右吹入空气进行吹炼。焙砂中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式是 、___________________________;
(7)假定各步反应都完全,完成下列计算:
①由6 mol CuFeS2生成6 mol Cu,求消耗O2的物质的量 mol;
② 6 mol CuFeS2和14.25 mol O2反应,理论上可得到 molCu。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是
A、X与Y形成化合物是,X可以显负价,Y显正价
B、气态氢化物的稳定性:HmY小于HnX
C、第一电离能可能Y小于X
D、最高价含氧酸的酸性:X对应的酸的酸性弱于Y对应的酸的酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.同温同压下,相同体积的物质,其物质的量一定相等
B.不同的外界条件下,等物质的量的甲烷和一氧化碳所含的分子数不一定相等
C.1 L一氧化碳气体一定比1 L氧气的质量小
D.相同条件下的一氧化碳气体和氮气,若体积相等,则分子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应N2(g)+3H2(g)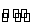 2NH3(g)(正反应为放热反应),下列说法中正确的是( )
2NH3(g)(正反应为放热反应),下列说法中正确的是( )
A.达到平衡后加入N2,当重新达到平衡时,NH3的浓度比原平衡的大,H2的浓度比原平衡的小
B.达到平衡后,升高温度,既加快了正、逆反应速率,又提高了NH3的产率
C.达到平衡后,缩小容器体积,既有利于加快正、逆反应速率,又有利于提高氢气的转化率
D.加入催化剂可以缩短达到平衡的时间,是因为正反应速率增大了,而逆反应速率减小了
查看答案和解析>>
科目:高中化学 来源: 题型:
为了配制NH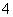 与Cl-的浓度比为1∶1的溶液,可在NH4Cl溶液中加入( )
与Cl-的浓度比为1∶1的溶液,可在NH4Cl溶液中加入( )
①适量HCl ②适量NaCl ③适量氨水 ④适量NaOH
A.①② B.③ C.③④ D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:

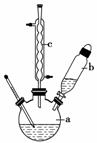
制备苯乙酸的装置示意图如右(加热和夹持装置等略):
已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL 70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是________________________。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器b的作用是____________________________________________;
仪器c的名称是__________________________,其作用是______________________________。反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是________________________。下列仪器中可用于分离苯乙酸粗品的是________(填标号)。
A.分液漏斗 B.漏斗
C.烧杯 D.直形冷凝管
E.玻璃棒
(3)提纯粗苯乙酸的方法是________________,最终得到44 g纯品,则苯乙酸的产率是________________。
(4)用CuCl2·2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是________________________________。
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30 min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
固定和利用CO2能有效地利用资源,并减少空气中的温室气体。CO2与化合物Ⅰ反应生成化合物Ⅱ,与化合物Ⅲ反应生成化合物Ⅳ,如反应①和②所示(其他试剂、产物及反应条件均省略)。
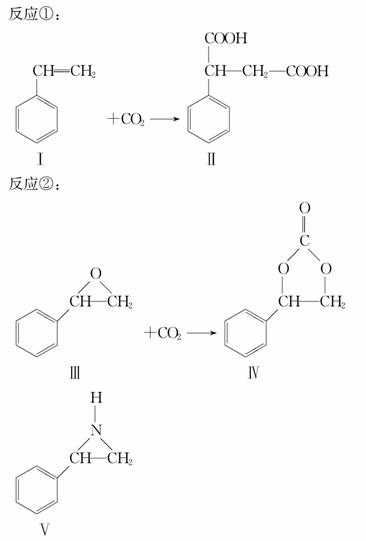
(1)化合物Ⅰ的分子式为 ,1 mol该物质完全燃烧需消耗 mol O2。
(2)由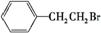 通过消去反应制备Ⅰ的化学方程式为 (注明反应条件)。
通过消去反应制备Ⅰ的化学方程式为 (注明反应条件)。
(3)Ⅱ与过量C2H5OH在酸催化下发生酯化反应,生成的有机物的结构简式为 。
(4)在一定条件下,化合物Ⅴ能与CO2发生类似反应②的反应,生成两种化合物(互为同分异构体),请写出其中任意一种化合物的结构简式: 。
(5)与CO2类似,CO也能被固定和利用。在一定条件下,CO、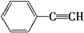 和H2三者发生反应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应。下列关于Ⅵ和Ⅶ的说法正确的有 (双选,填字母)。
和H2三者发生反应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应。下列关于Ⅵ和Ⅶ的说法正确的有 (双选,填字母)。
A.都属于芳香烃衍生物
B.都能使溴的四氯化碳溶液褪色
C.都能与Na反应放出H2
D.1 molⅥ或Ⅶ最多能与4 mol H2发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com