
高锰酸钾(KMnO4)和过氧化氢(H2O2)是两种典型的氧化剂。
(1)H2O2的结构式为________________。
(2)下列物质中能使酸性KMnO4溶液褪色的是________(填序号)。
A.臭碱(Na2S) B.小苏打(NaHCO3)
C.水玻璃(Na2SiO3) D.酒精(C2H5OH)
(3)高锰酸钾、双氧水、活性炭常用于饮用水的处理,但三者联合作用时必须有先后顺序。
①在稀硫酸中,KMnO4和H2O2能发生氧化还原反应:
氧化反应:H2O2-2e-—→2H++O2↑
还原反应:MnO +5e-+8H+—→Mn2++4H2O
+5e-+8H+—→Mn2++4H2O
写出该氧化还原反应的离子方程式:____________________________。
②在处理饮用水时,活性炭应在高锰酸钾反应结束后投加,否则会发生反应:KMnO4+C+H2O—→MnO2+X+K2CO3(未配平),其中X的化学式为________。
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中能大量共存的是( )
A.pH =1的溶液中:K+、Fe2+、MnO
=1的溶液中:K+、Fe2+、MnO 、SO
、SO
B.c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO 、SCN-
、SCN-
C.c(H+)/c(OH-)=1012的溶液中:NH 、Al3+
、Al3+ 、NO
、NO 、Cl-
、Cl-
D.与铝反应生成氢气的溶液中:NH 、K+、Cl-、SiO
、K+、Cl-、SiO
查看答案和解析>>
科目:高中化学 来源: 题型:
关于如图所示各装置的叙述中,正确的是( )
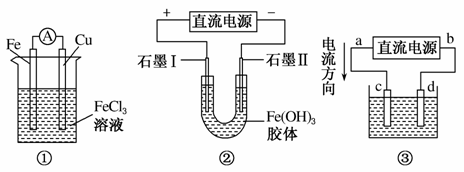
A.装置①是原电池,总反应是Cu+2Fe3+===Cu2++2Fe2+
B.装置①中,铁作负极,负极反应式为Fe3++e-===Fe2+
C.装置②通电一段时间后石墨Ⅱ电极附近溶液红褐色加深
D.若用装置③精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及 少量杂质铁,利用电解法可回收WC和Co。工艺流程简图如下:
少量杂质铁,利用电解法可回收WC和Co。工艺流程简图如下:
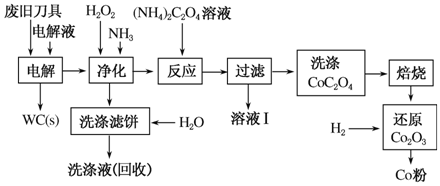
(1)电解时废旧刀具作阳极,不锈钢作阴极,HCl溶液为电解液。阴极主要的电极反应式为________。
(2)净化步骤所得滤饼的主要成分是________。回收的洗涤液代替水配制电解液,目的是回收利用其中的________。
(3)溶液Ⅰ的主要成分是________。洗涤CoC2O4不充分对最终产品纯度并无明显影响,但焙烧时会造成环境污染,原因是______________。
(4)将Co2O3还原成Co粉的化学反应方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象及相关的离子方程式均正确的是( )
A.碳酸钙粉末中加入醋酸溶液,固体逐渐减少,生成无色气体:CaCO3+2H+===Ca2++CO2↑+H2O
B.向BaCl2溶液中通入SO2气体,出现白色沉淀:Ba2++SO2+H2O===BaSO3↓+2H+
C.向H2O2溶液中滴加酸化的KMnO4溶液,KMnO4溶液褪色:2MnO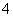 +7H2O2+6H+===2Mn2++6O2↑+10H2O
+7H2O2+6H+===2Mn2++6O2↑+10H2O
D.将等物质的量浓度、等体积的Ba(OH)2溶液和NaHSO4溶液混合,生成白色沉淀:Ba2++SO +H++OH-===BaSO4↓+H2O
+H++OH-===BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列区分植物油和矿物油的方法中,正确的是( )
A.点燃,能燃烧的为矿物油
B.加入水中,浮在水面上的为植物油
C.加入足量的NaOH溶液共煮,不再分层的为植物油
D.尝一尝,能食用的为植物油
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是制备CuO的流程图:
工业CuSO4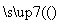
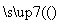 CuSO4溶液
CuSO4溶液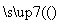 CuSO4·5H2O—→……—→CuO
CuSO4·5H2O—→……—→CuO
(1)步骤Ⅰ的目的是除去不溶性杂质。操作是_________________________________。
(2)步骤Ⅱ的目的是除铁。操作是:滴加H2O2溶液,稍加热;当Fe2+转化完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制 溶液pH=3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1。控制溶液pH=3.5的原因是___________________________
溶液pH=3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1。控制溶液pH=3.5的原因是___________________________
________________________________________________________________________。
(3)步骤Ⅲ的目的是得到CuSO4·5H2O晶体。操作是_____________________________
____________________________________________________________(填操作名称),
过滤,水浴加热烘干。水浴加热的特点是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下实验能获得成功的是
A.用乙醇和乙酸混合共热制取乙酸乙酯
B.将铁屑、溴水、苯混合制溴苯
C.在苯中滴入浓硝酸制硝基苯
D.将铜丝在酒精灯加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com