
| A. | 28g乙烯的气体中含有H原子数为2NA | |
| B. | 标准状况下,2.24L乙醇与足量Na反应生成H2分子数0.05NA | |
| C. | 每摩尔-OH中含电子数目为9NA | |
| D. | 每摩尔苯中含有的碳碳双键的数目为3NA |
分析 A.乙烯分子中含有4个H原子,28g乙烯的物质的量为1mol,含有4molH原子;
B.标准状况下,乙醇的状态不是气体;
C.羟基中含有9个电子,1mol羟基中含有9mol电子;
D.苯分子中的碳碳键为一种独特键,不存在碳碳双键.
解答 解:A.28g乙烯的物质的量为:$\frac{28g}{28g/mol}$=1mol,1mol乙烯分子中含有4molH原子,含有H原子数为4NA,故A错误;
B.标况下乙醇不是气体,不能使用标况下的气体摩尔体积计算,故B错误;
C.1mol羟基中含有9mol电子,1mol-OH中含电子数目为9NA,故C正确;
D.苯分子中的碳碳键为一种介于单键和双键之间的独特键,不存在碳碳双键,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的计算和判断,题目难度中等,注意熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间关系,明确标况下气体摩尔体积的使用条件,C注意羟基与氢氧根离子的区别.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制的氯水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈橙色 |
| ② | 向盛有少量碘化钾溶液的试管中滴加少量溴水,振荡,再注入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 进入煤矿井时,用火把照明 | |
| B. | 用点燃的火柴在液化气钢瓶旁检验钢瓶是否漏气 | |
| C. | 将氧气和氢气的混合气体通过灼热的氧化铜,以除去其中的氢气 | |
| D. | 某地化工厂的贮藏罐肆意外发生泄漏,有关方面紧急组织群众沿逆风方向疏散 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙炔的结构简式:C2H2 | |
| B. | S2-的结构示意图: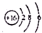 | |
| C. | 甲烷分子的球棍模型 | |
| D. | 硫酸钠的电离方程式:Na2S04=2Na++S042- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
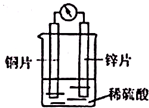
| A. | 溶液中H+向锌极移动 | |
| B. | 铜片是正极,发生氧化反应,有气泡产生 | |
| C. | 锌片上的电极反应式:Zn-2e-═Zn2+ | |
| D. | 电子由铜片经导线流向锌片 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2、H2和NH3的质量分数不再改变 | |
| B. | c(N2):c(H2):c(NH3)=1:3:2 | |
| C. | 单位时间里每增加1molN2,同时减少2mol NH3 | |
| D. | 单位时间里每增加1molN2,同时增加3molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
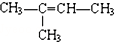
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
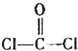 的空间结构为平面三角形.
的空间结构为平面三角形.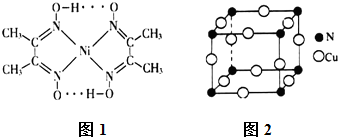
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com