
| A. | 可以用pH试纸测饱和氯水的pH | |
| B. | 用量筒量取8.61 mL 0.1 mol•L-1盐酸 | |
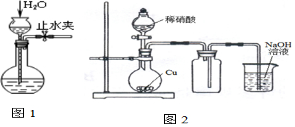
| C. | 用图1所示的操作检查装置的气密性 | |
| D. | 实验室用图2所示的装置制取少量的NO |
分析 A.氯水具有强氧化性,无法用pH试纸测饱和氯水的pH;
B.量筒的最小读数为0.1mL;
C.利用长颈漏斗中液柱的高度检验气密性;
D.不能用排空气收集NO.
解答 解:A.氯水中含有次氯酸,具有漂白性,无法用pH试纸测饱和氯水的pH,故A错误;
B.量筒只能读到0.1mL,无法用量筒量取8.61 mL 0.1 mol•L-1盐酸,故B错误;
C.关闭止水夹,观察长颈漏斗中液柱的高度检验气密性,故C正确;
D.NO与空气中氧气反应,能用排空气收集NO,故D错误;
故选C.
点评 本题考查化学实验方案的评价,涉及pH的测定、仪器使用、气密性检验、气体的制取及收集等,侧重基础知识的考查,注意物质的性质及化学反应原理,题目难度不大,选项A为易错点.


 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 至少存在5种离子 | |
| B. | Cl-一定存在,且 c (Cl-)>0.4mol/L | |
| C. | SO42-、NH4+、一定存在,Cl-可能不存在 | |
| D. | CO32-、Al3+-定不存在,K+可能存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 集中处理废旧电池,以防止重金属污染 | |
| B. | 食用含铁丰富的食物,可预防缺铁性贫血 | |
| C. | 使用加碘食盐,可预防因缺碘引起的甲状腺肿大 | |
| D. | 大量使用食品添加剂,可使食品营养更丰富 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
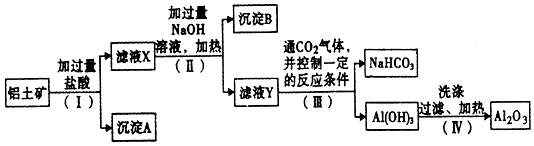
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用滴管滴加液体时,为防止液体滴到试管外面,滴管应紧贴管内壁 | |
| B. | 量筒里装一定量水,沿时筒内壁缓缓倒入浓硫酸,边倒边搅拌,配制稀硫酸 | |
| C. | 皮肤上不慎沾洒上了浓硫酸,应先用水冲洗,再涂上一层氢氧化钠溶液 | |
| D. | 称量易潮解的药品时药品应放在小烧杯等容器中称量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
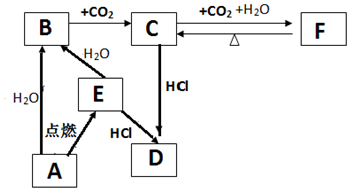
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com