
| A. | 短周期元素形成离子后,最外层都达到8电子稳定结构 | |
| B. | 检验铵盐方法:加氢氧化钠溶液,加热,用蘸有浓硫酸的玻璃棒靠近瓶口 | |
| C. | .制取硝酸铝方法:用AlCl3溶液和氨水反应,过滤得沉淀,再加稀HNO3 | |
| D. | 等物质的量的Na2CO3和NaHCO3分别与足量盐酸反应,后者放出的CO2多 |
分析 A.H原子失去电子后没有电子;
B.浓硫酸不挥发,无法检验是否有氨气生成;
C.氯化铝与氨水反应生成氢氧化铝沉淀,氢氧化铝与稀硝酸反应生成硝酸铝;
D.碳酸钠和碳酸氢钠的物质的量相等,根据C原子守恒可知生成二氧化碳的量相等.
解答 解:A.H为短周期元素,H原子只有一个电子,当H原子失去一个电子后没有电子,不满足8电子稳定结构,故A错误;
B.浓硫酸不具有挥发性,可用浓盐酸,正确的检验铵盐方法为:加氢氧化钠溶液,加热,用蘸有浓盐酸的玻璃棒靠近瓶口,故B错误;
C.氨水为弱碱,用AlCl3溶液和氨水反应生成氢氧化铝沉淀,过滤得氢氧化铝,再加稀HNO3可获得硝酸铝,故C正确;
D.等物质的量的Na2CO3和NaHCO3分别与足量盐酸反应,所有C元素都转化成二氧化碳,则二者放出的CO2的量相等,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质检验与制备、碳酸钠、碳酸氢钠的性质等知识,侧重实验基本操作和反应原理的考查,注意实验操作的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题

| A. | a电极是该电池的负极,发生氧化反应 | |
| B. | b电极反应式为2NO3-+10e-+12H+═N2↑+6H2O | |
| C. | 电池工作时,H+由左室通过质子交换膜进入右室 | |
| D. | 转化室中发生反应后溶液的pH增大(忽略体积变化) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
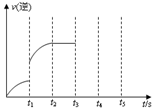 一定温度下在体积为5L的密闭容器中发生某可逆反应,其化学平衡常数表达式为:$K=\frac{{c(CO)•c({H_2})}}{{c({H_2}O)}}$
一定温度下在体积为5L的密闭容器中发生某可逆反应,其化学平衡常数表达式为:$K=\frac{{c(CO)•c({H_2})}}{{c({H_2}O)}}$查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水蒸气、液态水和冰中,水分子都在不停地运动 | |
| B. | NaCl溶于水后,因为共价键被破坏,从而形成了Na+和Cl- | |
| C. | 在N2、CO2和SiO2物质中,都存在共价键,它们都是由分子构成 | |
| D. | H2S分子中,所有原子的最外层都达到了8电子的稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是离子化合物,含有离子键和共价键 | |
| B. | 电子式是: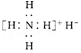 | |
| C. | 与水反应时,氢化铵被氧化 | |
| D. | 固体投入少量的水中,有两种气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石和石墨互为同分异构体,熔点和硬度都很高 | |
| B. | 12C、13C、14C是碳元素的三种核素,互称为同位素 | |
| C. | 乙醇和二甲醚(CH3-O-CH3)互为同系物 | |
| D. | C4H10的一氯代物只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2C O (g)+O2(g)═2CO2(g) | B. | HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l) | ||
| C. | 2H2(g)+O2(g)═2H2O(l) | D. | Zn(s)+Ag2 O(s)═Zn O(s)+2Ag(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
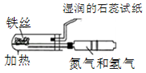 | 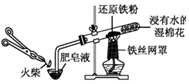 |
| A.模拟工业制氨气并检验产物 | B.一段时间后,试管中固体变为红棕色 |
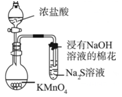 | 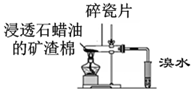 |
| C.可用所示装置比较KMnO4、Cl2、S的氧化性强弱 | D.若溴水褪色则证明石蜡油分解产生乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com