

·ÖĪö £Ø1£©øõĢśæó¼ÓČėĢ¼ĖįÄĘ£¬ĶØČėŃõĘų±ŗÉÕ·¢Éś·“Ӧɜ³ÉŃõ»ÆĢś”¢Na2CrO4ŗĶ¶žŃõ»ÆĢ¼£¬½įŗĻŌ×ÓŹŲŗćŗĶµē×ÓŹŲŗćÅäĘ½ŹéŠ“»Æѧ·½³ĢŹ½£»²½Öč¢ń¼ÓČėĖ®Čܽā£¬·ÖĄė¹ĢĢåŗĶČÜŅŗÓĆ¹żĀĖ£»
£Ø2£©²½Öč¢ņÖŠæɼÓČėNa2SČÜŅŗŹµĻÖ×Ŗ»Æ£¬·“Ó¦ŗóµÄĀĖŅŗÖŠÓŠNa2S2O3£¬Éś³ÉCr£ØOH£©3”ż³Įµķ£¬½įŗĻŌ×ÓŹŲŗćŗĶµē×ÓŹŲŗćÅäĘ½ŹéŠ“»Æѧ·½³ĢŹ½£¬CrŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+6¼Ū±äĪŖ+3¼Ū£»
£Ø3£©µē½āČŪȌדĢ¬µÄCr2O3£¬Ńō¼«ÉĻŃõĄė×ÓŹ§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬Ņõ¼«ÉĻøõĄė×ӵƵē×Ó·¢Éś»¹Ō·“Ó¦£»
£Ø4£©ŌŚ60”ęŅŌÉĻÕō·¢ČܼĮ£¬NaClČܽā¶Č×īŠ”£¬Ņ׳Įµķ£¬ŅņK2Cr2O7Čܽā¶ČĖęĪĀ¶Č±ä»Æ½Ļ“ó£¬Č”ĀĖŅŗ½µĪĀ½į¾§£¬¼“µĆK2Cr2O7¾§Ģ壻
£Ø5£©øł¾ŻCr£ØOH£©3µÄKsp=6.3”Į10-31=c£ØCr3+£©”Įc3£ØOH-£©¼ĘĖć£®
½ā“š ½ā£ŗ£Ø1£©øõĢśæó¼ÓČėĢ¼ĖįÄĘ£¬ĶØČėŃõĘų±ŗÉÕ·¢Éś·“Ӧɜ³ÉŃõ»ÆĢś”¢Na2CrO4ŗĶ¶žŃõ»ÆĢ¼£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ8Na2CO3+4Fe£ØCrO2£©2+7O2$\frac{\underline{\;ģŃÉÕ\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2”ü£¬²½Öč¢ń¼ÓČėĖ®Čܽā£¬·ÖĄė¹ĢĢåŗĶČÜŅŗÓĆ¹żĀĖ£¬²½Öč¢ńÉę¼°µÄ²Ł×÷ÓŠČܽā”¢¹żĀĖ£¬
¹Ź“š°øĪŖ£ŗ8Na2CO3+4Fe£ØCrO2£©2+7O2$\frac{\underline{\;ģŃÉÕ\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2”ü£»Čܽā”¢¹żĀĖ£»
£Ø2£©²½Öč¢ņÖŠæɼÓČėNa2SČÜŅŗŹµĻÖ×Ŗ»Æ£¬·“Ó¦ŗóµÄĀĖŅŗÖŠÓŠNa2S2O3£¬Éś³ÉCr£ØOH£©3”ż³Įµķ£¬CrŌŖĖŲµÄ»ÆŗĻ¼ŪÓÉ+6¼Ū±äĪŖ+3¼Ū£¬ĮņŌŖĖŲ-2¼Ū±ä»ÆĪŖ+2¼Ū£¬½įŗĻµē×ÓŹŲŗćŗĶµēŗÉŹŲŗć”¢Ō×ÓŹŲŗćÅäĘ½ŹéŠ“µĆµ½Ąė×Ó·½³ĢŹ½£ŗ8CrO42-+6S2-+23H2OØT8Cr£ØOH£©3”ż+3S2O32-+22OH-£¬
¹Ź“š°øĪŖ£ŗ8CrO42-+6S2-+23H2OØT8Cr£ØOH£©3”ż+3S2O32-+22OH-£»
£Ø3£©µē½āČŪȌדĢ¬µÄCr2O3£¬Ńō¼«ÉĻŃõĄė×ÓŹ§µē×ÓÉś³ÉŃõĘų£¬Ņõ¼«ÉĻøõĄė×ӵƵē×Ó·¢Éś»¹Ō·“Ó¦£¬ĖłŅŌŃō¼«ÉĻµē¼«·“Ó¦Ź½ĪŖ£ŗ2O2--4e-=O2”ü£¬
¹Ź“š°øĪŖ£ŗ2O2--4e-=O2”ü£»
£Ø4£©K2Cr2O7æÉÓÉKClŗĶNa2Cr2O7·“Ó¦ÖĘµĆ£¬øł¾ŻĶ¼2ĖłŹ¾Čܽā¶ČĒśĻßĶ¼£¬ÄÜÖĘČ”K2Cr2O7¾§ĢåµÄŌŅņŹĒ£ŗŌŚ60”ęŅŌÉĻÕō·¢ČܼĮ£¬NaClČܽā¶Č×īŠ”£¬Ņ׳Įµķ£¬“Ó¶ųŹ¹·“Ó¦KCl+Na2Cr2O7ØTK2Cr2O7+2NaCl”ż ·¢Éś£¬ŅņK2Cr2O7Čܽā¶ČĖęĪĀ¶Č±ä»Æ½Ļ“ó£¬Č”ĀĖŅŗ½µĪĀ½į¾§£¬¼“µĆK2Cr2O7¾§Ģ壬
¹Ź“š°øĪŖ£ŗŌŚ60”ęŅŌÉĻÕō·¢ČܼĮ£¬NaClČܽā¶Č×īŠ”£¬Ņ׳Įµķ£¬“Ó¶ųŹ¹·“Ó¦KCl+Na2Cr2O7ØTK2Cr2O7+2NaCl”ż ·¢Éś£¬ŅņK2Cr2O7Čܽā¶ČĖęĪĀ¶Č±ä»Æ½Ļ“ó£¬Č”ĀĖŅŗ½µĪĀ½į¾§£¬¼“µĆK2Cr2O7¾§Ģ壻
£Ø5£©ČōµŲ±ķĖ®øõŗ¬Įæ×īøßĻŽÖµŹĒ0.1mg/L£¬»»Ėć³ÉĪļÖŹµÄĮæÅضČc£ØCr3+£©=$\frac{1”Į1{0}^{-4}}{52}$mol/L£¬ŅŖŹ¹ČÜŅŗÖŠc£ØCr3+£©½µµ½·ūŗĻµŲ±ķĖ®ĻŽÖµ£¬ŅŃÖŖCr£ØOH£©3µÄKsp=6.3”Į10-31=c£ØCr3+£©”Įc3£ØOH-£©£¬Šėµ÷½ŚČÜŅŗµÄc£ØOH-£©”Ż$\root{3}{\frac{6.3”Į1{0}^{-31}}{\frac{1”Į1{0}^{-4}}{52}}}$mol/L£¬
¹Ź“š°øĪŖ£ŗ$\root{3}{\frac{6.3”Į1{0}^{-31}}{\frac{1”Į1{0}^{-4}}{52}}}$£®
µćĘĄ ±¾Ģāæ¼²é½ĻĪŖ×ŪŗĻ£¬Éę¼°Ńõ»Æ»¹Ō·“Ó¦”¢µē½āŌĄķ”¢»Æѧ·½³ĢŹ½ŹéŠ“”¢ĪļÖŹ·ÖĄėĢį“æµČÖŖŹ¶µć£¬ŠčŅŖѧɜ¾ß±øŌśŹµµÄ»ł“”ÖŖŹ¶£¬Ę½Ź±×¢ŅāÅąŃų·ÖĪöŗĶ½ā¾öĪŹĢāµÄÄÜĮ¦£¬ĢāÄæÄѶČÖŠµČ£®


 ŗ®¼ŁĢģµŲÖŲĒģ³ö°ęÉēĻµĮŠ“š°ø
ŗ®¼ŁĢģµŲÖŲĒģ³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ŹŌ¹ÜbÖŠµ¼Ęų¹ÜĻĀ¶Ė¹ÜæŚ²»ÄܽžČėŅŗĆęµÄÄæµÄŹĒ·ĄÖ¹ŹµŃé¹ż³ĢÖŠ²śÉśµ¹ĪüĻÖĻó | |
| B£® | ĻņaŹŌ¹ÜÖŠĻČ¼ÓČėÅØĮņĖį£¬Č»ŗó±ßŅ”¶ÆŹŌ¹Ü±ßĀżĀż¼ÓČėŅŅ“¼£¬ŌŁ¼ÓČė±ł“×Ėį | |
| C£® | 1molŅŅĖįÓė1molŅŅ“¼³ä·Ö·“Ó¦“ļĻŽ¶ČŹ±£¬µĆµ½µÄŅŅĖįŅŅõ„Š”ÓŚ1mol | |
| D£® | ŹŌ¹ÜbÖŠ±„ŗĶNa2CO3ČÜŅŗµÄ×÷ÓĆŹĒĪüŹÕĖęŅŅĖįŅŅõ„Õō³öµÄÉŁĮæŅŅĖįŗĶŅŅ“¼ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šŹōÄĘ×Å»šæÉÓƶžŃõ»ÆĢ¼ĘĖĆš | |
| B£® | ½«¶žŃõ»Æ¹čČÜÓŚĖ®æÉÖĘµĆ¹čĖį½ŗĢå | |
| C£® | ŗę±ŗŹ³Ę·Ź±¼ÓČėŠ”ĖÕ“ņæÉŅŌŹ¹Ź³Ę·ÅīĖÉ | |
| D£® | ÓĆŃõ»ÆĀĮÖĘ³ÉµÄŪįŪöæÉÓĆÓŚ¼ÓČČæĮŠŌÄĘ¹ĢĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 45 mL | B£® | 50 mL | C£® | 30 mL | D£® | 60 mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²ĻĖ攢ČĖŌģĖæ³ä·ÖĖ®½āŗó¾łæɵƵ½°±»łĖį | |
| B£® | øÕÓń”¢ŗģ±¦ŹÆÖ÷ŅŖ³É·Ö¶¼ŹĒŃõ»ÆĀĮ£¬ĢÕ“É”¢·Ö×ÓÉø”¢Ė®¾§Ö÷ŅŖ³É·Ö¶¼ŹĒ¹čĖįŃĪ | |
| C£® | ²ÉČ””°¾²µē³ż³¾”±·½·Ø¾»»ÆæÕĘų£¬ĄūÓĆĮĖ½ŗĢåµÄĻą¹ŲÖŖŹ¶ | |
| D£® | ŌöĖܼĮDNOP£ØĮŚ±½¶ž¼×Ėį¶žŠĮõ„£©ŅņÓŠĢŲŹāĻćĪ¶£¬Ņ²æÉÓĆ×÷Ź³Ę·Ģķ¼Ó¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ¹āÄÜ“¢“ęŅ»°ćŹĒÖø½«¹āÄÜ×Ŗ»»ĪŖµēÄÜ»ņ»ÆѧÄܽųŠŠ“¢“ę£¬ĄūÓĆĢ«Ńō¹ā”¢CO2”¢H2OÉś³É¼×“¼µÄ¹āÄÜ“¢“ę×°ÖĆČēĶ¼ĖłŹ¾£¬ÖʱøæŖŹ¼Ź±ÖŹ×Ó½»»»Ä¤Į½²ąµÄČÜŅŗÖŹĮæĻąµČ£®ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø””””£©
¹āÄÜ“¢“ęŅ»°ćŹĒÖø½«¹āÄÜ×Ŗ»»ĪŖµēÄÜ»ņ»ÆѧÄܽųŠŠ“¢“ę£¬ĄūÓĆĢ«Ńō¹ā”¢CO2”¢H2OÉś³É¼×“¼µÄ¹āÄÜ“¢“ę×°ÖĆČēĶ¼ĖłŹ¾£¬ÖʱøæŖŹ¼Ź±ÖŹ×Ó½»»»Ä¤Į½²ąµÄČÜŅŗÖŹĮæĻąµČ£®ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | nŠĶ°ėµ¼ĢåĪŖøŗ¼« | |
| B£® | X2ĪŖO2£¬H+ÓÉb¼«Ļņa¼«ŅĘ¶Æ | |
| C£® | b¼«µÄµē¼«·“Ó¦Ź½ĪŖCO2+6e-+6H+=CH3OH+H2O | |
| D£® | µ±Öʱø32g¼×“¼Ź±£¬ÖŹ×Ó½»»»Ä¤Į½²ąČÜŅŗĻą²ī104g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
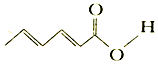
| A£® | ·Ö×ÓŹ½ĪŖC6H8O2 | |
| B£® | æÉŹ¹KMnO4£ØH+£©ČÜŅŗĶŹÉ« | |
| C£® | 1 mol øĆĪļÖŹ×ī¶ąæÉÓė3 mol Br2 ·¢Éś¼Ó³É·“Ó¦ | |
| D£® | æÉÓė“¼·¢ÉśČ”“ś·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶žŃõ»ÆĢ¼ÓėĒæ¼īČÜŅŗ·“Ó¦ | B£® | ŠæŗĶĮņĖį·“Ó¦ | ||
| C£® | ĢśŗĶĀČĘų·“Ó¦ | D£® | ĀČ»ÆĀĮČÜŅŗŗĶÉÕ¼īČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com