
| c(X)/ mol·L-1 | c(Y)/ mol·L-1 | v/ mol·L-1·s-1 |
1 | 0.10 | 0.10 | 4.0×10-4 |
2 | 0.20 | 0.10 | 1.6×10-3 |
3 | 0.30 | 0.10 | 3.6×10-3 |
4 | 0.30 | 0.20 | 7.2×10-3 |
根据以上实验数据,完成下列问题:
(1)上述反应在
(2)当c(X)=c(Y)=0.25 mol·L-1时,v=_______________。
科目:高中化学 来源: 题型:
 某同学设计了如图所示装置(部分夹持装置已略去)进行实验研究.
某同学设计了如图所示装置(部分夹持装置已略去)进行实验研究.| 序号 | V(H2SO4)/mL | c(H2SO4)/mol?L-1 | t/s | Ⅰ | 40 | 1 | t1 | Ⅱ | 40 | 4 | t2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 8 |
- 3 |
2- 4 |
- 3 |
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol?L | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82-)/mol?L | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学设计了如图所示装置(部分夹持装置已略去)进行实验研究.请回答:
某同学设计了如图所示装置(部分夹持装置已略去)进行实验研究.请回答:| 序号 | V(H2SO4)/mL | C(H2SO4)/mol?L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 4 | t2 |
查看答案和解析>>
科目:高中化学 来源:导学大课堂必修二化学鲁科版 鲁科版 题型:058
化学反应速率与反应物浓度的关系式(称为速率方程)是通过实验测定的,以反应aA+Dd![]() eE为例,可先假设该反应的速率方程为v=kcm(A)cn(D),然后通过实验测得的数据,算出k、m、n的值,再将k、m、n的值代入上式,即得速率方程.现测得25℃时溶液中的反应3X+2Y
eE为例,可先假设该反应的速率方程为v=kcm(A)cn(D),然后通过实验测得的数据,算出k、m、n的值,再将k、m、n的值代入上式,即得速率方程.现测得25℃时溶液中的反应3X+2Y![]() 2Z在不同浓度时的反应速率如下表:
2Z在不同浓度时的反应速率如下表:
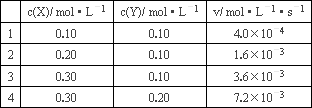
根据以上实验数据,完成下列问题:
(1)上述反应在25℃时的速率方程为v=________.
(2)当c(X)=c(Y)=0.25 mol·L-1时,v=________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com