
���� ��1��Ԫ�صĻ��ϼ����ߣ�����ԭ����Ԫ�صĻ��ϼ۽��ͣ�����������
��2��ά����C����ʹʳ���е�Fe3+��ԭ��Fe2+��FeԪ�صĻ��ϼ۽��ͣ�����������ά���ؿɸ������ܽ��ԵIJ�ͬ��Ϊ֬����ά���غ�ˮ����ά���������ࣻ
��3���������ᷴӦ�����Ȼ�������������
��� �⣺��1��Fe2+��Fe3+��ת��ʱ��FeԪ�صĻ��ϼ����ߣ�Fe2+����ԭ����Fe3+��Fe2+ת��ʱ��FeԪ�صĻ��ϼ۽��ͣ�Fe3+����������
�ʴ�Ϊ����ԭ��������
��2��ά����C����ʹʳ���е�Fe3+��ԭ��Fe2+��FeԪ�صĻ��ϼ۽��ͣ�������������ά����C���л�ԭ�ԣ�����ԭ����ά���ؿɸ������ܽ��ԵIJ�ͬ��Ϊ֬����ά���غ�ˮ����ά���������ࣻά����C��ˮ����ά���أ�
�ʴ�Ϊ����ԭ��֬�ܣ�ˮ�ܣ�ˮ�ܣ�
��3������������θ�ᣨ��Ҫ�ɷ�ʱ���ᣩ��������ת���������εĻ�ѧ��ӦΪFe+2H+=Fe2++H2����
�ʴ�Ϊ��Fe+2H+=Fe2++H2����
���� ���⿼��������ԭ��Ӧ��ά����C�����ʺ���;����ȷ������ԭ��Ӧ��Ԫ�صĻ��ϼ۱仯�ǽ����Ĺؼ�������Ϥ������ԭ��Ӧ�еĸ����������Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��һ�Ͻ�ѧ�ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
1mol/L NaCl��Һ��ʾ
A����Һ�ﺬ��1mol NaCl B��1mol NaCl�ܽ���1Lˮ��
C��58.5g NaCl����941.5gˮ�� D��1Lˮ��Һ�к���NaCl 58.5g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��������������ѧԺ���и߶����¿�����ѧ���������棩 ���ͣ�ѡ����
����˵����ӦP��g��+Q��g�� R��g��+S��s���ں��¡��������Ѵﵽƽ����ǣ� ��
R��g��+S��s���ں��¡��������Ѵﵽƽ����ǣ� ��
A����Ӧ�����ڵ�ѹǿ����ʱ��ı�
B����Ӧ������P��Q��R��S���߹���
C��P���������ʺ�S�������������
D����Ӧ�����ڵ����������ʵ�������ʱ��仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��������������ѧԺ���и߶����¿�����ѧ���������棩 ���ͣ�ѡ����
�������ȷ�Ӧ��˵������ȷ���ǣ� ��
A. ������ȵķ�Ӧһ�������ȷ�Ӧ B. ֻ�зֽⷴӦ�������ȷ�Ӧ
C. ʹ�ô����ķ�Ӧ�����ȷ�Ӧ D. ����кͷ�Ӧ���淴Ӧ�����ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
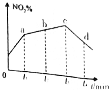 �о��������������ڴ����еĺ������ӵ������ʱ��������·�Ӧ��
�о��������������ڴ����еĺ������ӵ������ʱ��������·�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����¶Ⱥ�����������䣬���� 1 mol SO3��g�� | |
| B�� | �����¶Ⱥ�������ѹǿ���䣬���� 1 mol SO3��g�� | |
| C�� | �����¶Ⱥ�������ѹǿ���䣬���� 1 mol O2��g�� | |
| D�� | �����¶Ⱥ�������ѹǿ���䣬���� l mol Ar��g�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ�ҹ����ô����ϳɰ�������������� | |
| B�� | ��ѧ�Һϳ�̼���ܣ��������ӵ��ߺͳ�С�͵������� | |
| C�� | ������ѧ���Ž��з���Ԫ�������� | |
| D�� | ŵ���������������Ƴ���ըҩ�������ڹ�ҵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol �����к���12.04��1023����ԭ�ӣ��ڱ�״����ռ�����22.4 L | |
| B�� | 1 mol������1.5 mol����������ͬ����ԭ���� | |
| C�� | ��״���£�22.4 L H2O�ķ�����Ϊ1NA | |
| D�� | �����ʵ����ĸɱ��������ǣ�C6H12O6��������̼ԭ����֮��Ϊ1��6����ԭ����֮��Ϊ1��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ѹǿ��������Y��ת���ʼ�С | |
| B�� | ��XŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.001 mol/��L•s�� | |
| C�� | �������¶ȣ�X���������������÷�Ӧ�ġ�H��0 | |
| D�� | �����������Ϊ20 L��Z��ƽ��Ũ�ȱ�Ϊԭ����1/2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com