
���� ��1������A��Ũ�ȱ仯��������v=$\frac{��c��D��}{��t}$����v��A����
��2������ѹǿ��Ӧ��������Ӧǰ������Ļ�ѧ���������䣬ƽ�ⲻ�ƶ���
��3����Ӧ�����������ܵ����ʵ������䣬�¶�����ʱ��������ƽ����Է���������С��˵�������¶ȣ�����������������С��������Է�������M��B����3M��C�����������¶�ƽ�����淴Ӧ�����ƶ���
��� �⣺��1����c��A��=��c��D��=0.3mol/L����v��A��=$\frac{0.3mol/L}{2min}$=0.15mol/��L��min�����ʴ�Ϊ��0.15mol/��L��min����
��2������ѹǿ�����淴Ӧ���ʶ�����Ӧǰ������Ļ�ѧ���������䣬ƽ�ⲻ�ƶ���������D������������䣬�ʴ�Ϊ�������䣻
��3����Ӧ�����������ܵ����ʵ������䣬�¶�����ʱ��������ƽ����Է���������С��˵�������¶ȣ�����������������С��������Է�������M��B����3M��C�����������¶�ƽ�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ���ʴ�Ϊ�����ȣ�
���� ���⿼�黯ѧ��Ӧ���ʼ��㡢��ѧƽ����㼴Ӱ�����صȣ��ؼ��������Ӧǰ����������ʵ������䣬ѹǿ��Ӱ��ƽ���ƶ����Ѷ��еȣ�


 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��̿���м���KClO3����ȼʱȼ�ո�Ϊ���� | |
| B�� | п��ϡ���ᷴӦ�м�������CuSO4��Һ��ʹ��Ӧ�ų�H2�����ʼӿ� | |
| C�� | ˫��ˮ�м�������FeCl3���ɼӿ�ų���������� | |
| D�� | ��̬FeCl3����NaOH��Ϻ���ˮ��Ѹ�ٲ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
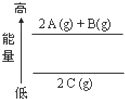
| A�� | 2A��g��+B��g��=2 C��g����H��0 | B�� | 2A��g��+B��g��=2 C��g����H��0 | C�� | 2C��g��=2A��g��+B��g����H��0 | D�� | 2C��g��=2 A��g��+B��g����H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��Na+��+c��H+��=c��X-��+c��OH-�� | |
| B�� | �����Һ�����ԣ���c��X-����c��Na+����c��HX����c��H+����c��OH-�� | |
| C�� | c��HX��+c��X-��=2c��Na+�� | |
| D�� | �����Һ�ʼ��ԣ���c��Na+����c��HX����c��X-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ba��OH��2��Һ�еμ�NaHSO4��Һ��ǡ��Ϊ���ԣ�Ba2++OH-+H++SO42-=BaSO4��+H2O | |
| B�� | NH4HCO3��Һ�����KOHŨ��Һ���ȣ�NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O | |
| C�� | ϡ�����������м��Ӧ��3 Fe+8H++2 NO3-=3 Fe3++2 NO��+4 H2O | |
| D�� | ����ʯ���ڴ���ķ�Ӧ��CaCO3+CH3COOH=Ca2++2CH3COO-+CO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | NaClO3�ڷ�Ӧ�л��ϼ۽��ͣ�ʧȥ���� | |
| B�� | SO2�ڷ�Ӧ�з���������Ӧ | |
| C�� | 2mol�������ڷ�Ӧ�еõ�2mol���� | |
| D�� | H2SO4�ڷ�Ӧ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeO��Fe2O3��Na2O2��Ϊ���������� | B�� | ϡ���������ᡢ�Ȼ�����Һ��Ϊ���� | ||
| C�� | �ռ�����ᡢ���Ȼ�̼��Ϊ����� | D�� | ���ᡢˮ��������ˮ��Ϊ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com