
| A. | 石油是混合物,其分馏产品汽油是纯净物 | |
| B. | 焰色反应有特征颜色出现,所以是化学反应 | |
| C. | 从海水中提取物质都必须通过化学反应才能实现 | |
| D. | 大量化石燃料是造成雾霾天气的一种重要因素 |
分析 A.石油是烃的混合物;
B.焰色反应是物理反应;
C.海水中提取氯化钠即为物理变化;
D.燃烧化石燃料可产生有害气体和烟尘.
解答 解:A.石油是烃的混合物,其分馏产品汽油也是烃的混合物,故A错误;
B.焰色反应的本质是原子内的电子获得能量后激发到能级较高的电子层,之后跃迁回原电子层时发出电磁波,当电磁波波长位于可见光范围内时即产生焰色反应,属于物理变化,故B错误;
C.海水中提取氯化钠没有新物质生成即为物理变化,故C错误;
D.大量燃烧化石燃料可产生有害气体和烟尘,是造成雾霾天气的一种重要因素,故D正确.
故选D.
点评 本题考查了物质分类方法常见生活环境的污染与治理、物理变化等问题,题目难度不大,学习中注意相关基础知识的积累.


科目:高中化学 来源: 题型:多选题
| A. | 溶液中一定有K+、Br-、CO32-、AlO2- | |
| B. | 溶液中一定没有Mg2+、Cu2+、Cl-、NH4+ | |
| C. | 不能确定溶液中是否有K+、SO42-、Cl- | |
| D. | 往第3份溶液中滴加BaCl2可确认是否有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 纯碱溶液能清洗油污:CO32-+H2O?HCO3-+OH- | |
| B. | 配制FeSO4溶液时加入适量的铁粉:Fe3++Fe→2Fe2+ | |
| C. | 含1molNaOH和1molNa2CO3的混合溶液中滴入含1.5molHCl的稀盐酸:2OH-+CO32-+3H+→HCO3-+2H2O | |
| D. | NH4Al(SO4)2溶液中滴入Ba(OH)2溶液至SO42-恰好沉淀完全:2Ba2++4OH-+Al3++2SO42-→2BaSO4↓+AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素 | 相关信息 |
| X | 元素周期表中核电荷数最小的元素 |
| y | Y的一种核素常用于考古,其一种同素异形体为自然界最硬的物质 |
| Z | Z是大气中含量多的元素,其某些氧化物为大气中常见的污染物 |
| W | W是地壳中含量最高的金属元素 |
| M | 常见金属,单质呈紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验组号 | ① | ② | ③ | ④ |
| 碳化物(g) | 6.2 | 9.3 | 15.5 | 21.7 |
| 水(mL) | 18 | 18 | 18 | 18 |
| 气体(L,标准状况) | 3.36 | 5.04 | 8.4左右 | 8.4左右 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素B、C、D的原子半径由大到小的顺序为:r(D)>r(C)>r(B) | |
| B. | C的单质在点燃条件分别与A、B、D的单质化合,所得化合物均存在共价键 | |
| C. | 四种元素的单质中,熔沸点最高的是D的单质 | |
| D. | C和D所形成离子的电子层结构一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 所用试剂 |
| A | 比较Fe3+和Cu2+的氧化性 | FeCl3溶液和Cu |
| B | 比较镁和铝的金属性 | MgCl2溶液、AlCl3溶液、NaOH溶液 |
| C | 比较硫和氯的非金属性 | 氢硫酸、氯气 |
| D | 比较苯酚和碳酸的酸性 | 0.1mol/L苯酚钠、0.1mol/L碳酸钠溶液pH试纸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向CuSO4溶液中加入适量铁粉 | B. | 等浓度等体积的(NH4)2SO4和BaCl2 | ||
| C. | 等物质的量的NaHCO3和Na2O2 | D. | 在NaBr溶液中通入过量的Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
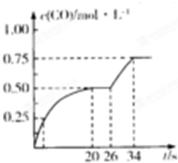 甲烷、甲醇、CO、H2、CO2均是重要的化工原料.
甲烷、甲醇、CO、H2、CO2均是重要的化工原料.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com