
| A、向氯化银的浊液中加入氯化钠溶液,氯化银的Ksp减小 |
| B、向2.0×10-4mol?L-1的K2CrO4溶液中加入等体积的2.0×10-4 mol?L-1 AgNO3溶液,则有Ag2CrO4沉淀生成 |
| C、将一定量的AgCl和Ag2CrO4固体混合物溶于蒸馏水中,充分溶解后,静置,上层清液中Cl-的物质的量浓度最大 |
| D、将0.001 mol?L-1的AgNO3溶液逐滴滴入0.001 mol?L-1的KCl和0.001 mol?L-1的K2CrO4的混合溶液中,则先产生AgCl沉淀 |
| 2.0×10-4 |
| 2 |
| 2.0×10-4 |
| 2 |
| Ksp(AgCl) |
| c(Cl-) |
|


科目:高中化学 来源: 题型:
 已知由 C、N、O、Na、Fe五种元素组成的常见单质或化合物存在如图所示转化关系(部分生成物和反应条件略去).
已知由 C、N、O、Na、Fe五种元素组成的常见单质或化合物存在如图所示转化关系(部分生成物和反应条件略去).查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、电解过程中,d电极质量增加 |
| B、d为阳极,电极反应为:2Cl--2e-=Cl2↑ |
| C、a为负极、b为正极 |
| D、电解过程中,氯离子浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、9:1 | B、18:7 |
| C、41:9 | D、1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、.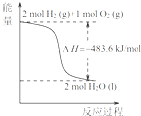 热化学方程式是H2(g)+
| ||
B、. 对于恒温恒容条件下的反应2NO2(g)?N2O4(g),A点为平衡状态 | ||
C、 将A、B饱和溶液分别由T1℃升温至T2℃时,溶质的质量分数B>A | ||
D、. 同温度、同浓度的NaA溶液与NaB溶液相比,其pH前者小于后者 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com