

分析 (1)电解质:在水溶液中或熔融状态下能够导电的化合物;
非电解质:在熔融状态和水溶液中都不能导电的化合物;
氧化物:氧元素与另外一种化学元素组成的二元化合物,据此进行判断;
(2)乙醇和二氧化碳都是含碳化合物,二者都是非电解质;
(3)根据题意分析得出两种物质间的关系,从而确定该物质,并写出相应的方程式;
(4)制备胶体的原理是利用铁离子水解生成氢氧化铁胶体.
解答 解:(1)CH3CH2OH不是氧化物;在水中和熔化状态下都不能导电,属于非电解质,
二氧化碳是氧化物;在水溶液中与水反应生成碳酸,二氧化碳自身不能电离,是非电解质,
Fe2O3是氧化物;在熔融状态下能够导电,属于电解质,
FeCl3不是氧化物;在水溶液中能够导电,属于电解质,
KOH不是氧化物;在水溶液中能够导电,属于电解质,
故相连的两种物质都是电解质的是CD;都是氧化物的是B;
故答案为:CD;B;
(2)a.乙醇和二氧化碳都属于非电解质,故a正确;
b.乙醇为有机物,而二氧化碳不属于有机物,故b错误;
c.乙醇和二氧化碳都是含碳化合物,故c正确;
d.二氧化碳为氧化物,而乙醇分子中含有H元素,不属于氧化物,故d错误;
故选ac;
(3)某一物质能与某种强酸反应生成上述中的另一种物质,所以这两种物质应有相同的元素,且化合价不变,所以是氧化铁和氯化铁,反应的离子方程式为:Fe2O3+6H+=2Fe3++3H2O,
故答案为:Fe2O3+6H+=2Fe3++3H2O;
(4)制备胶体的原理是利用铁离子水解生成氢氧化铁胶体,反应的离子方程式为Fe3++3H2O=Fe(OH)3(胶体)+3H+,故答案为:Fe3++3H2O=Fe(OH)3(胶体)+3H+.
点评 本题考查电解质和非电解质、氧化物概念的辨析、四种基本反应类型的判断、离子方程式的书写、胶体的制备等知识,液面难度中等,试题知识点较多,充分考查了学生的分析能力及灵活应用基础知识的能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
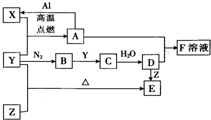 已知X、Y、Z为单质,其它为化合物.其中Y为气体,F溶液呈黄色,E是常见的温室气体,它们之间存在如下的转化关系(部分产物已经略去).请回答下列问题:
已知X、Y、Z为单质,其它为化合物.其中Y为气体,F溶液呈黄色,E是常见的温室气体,它们之间存在如下的转化关系(部分产物已经略去).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制乙烯和实验室制乙炔 | |
| B. | 乙烯使酸性高锰酸钾溶液褪色和乙醛使溴水褪色 | |
| C. | 苯酚制三溴苯酚和乙醛制乙醇 | |
| D. | 乙酸乙酯的水解和乙烯制聚乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 ,反应④的反应类型是消去反应.
,反应④的反应类型是消去反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 百分组成 NH3%=N2% | B. | 气体的密度不变 | ||
| C. | 压强不变 | D. | c(H2):c(N2):c(NH3)=3:1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com