
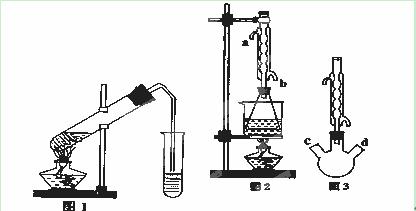
实验是化学研究的基础。下列关于各实验装置的叙述正确的是( )

A.装置①常用于分离互不相溶的液体混合物
B.装置②可用于吸收NH3或HCl气体,并防止倒吸
C.装置③可用于收集H2、CO2、Cl2、NH3等气体
D.装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
下列说法正确的是
A.ΔH<0、ΔS>0的反应在温度低时不能自发进行
B.NH4HCO3(s)===NH3(g)+H2O(g)+CO2(g);ΔH=+185.57 kJ/mol能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向
C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据
D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数。下列叙述正确的是……………( )
A.1mol乙烯分子中含有的共用电子对的数目为5NA
B.42g乙烯与丙烯的混合气体中含碳原子数为3NA
C.标准状况下,22.4L己烷中碳碳键数目为5NA
D.乙烯和乙醇的混合物共0.1mol,完全燃烧所消耗的氧分子数一定为0.6 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
制备乙酸乙酯的绿色合成路线之一为:

下列说法不正确的是( )
A.M的分子式为C6H12O6
B.用NaOH溶液可除去乙酸乙酯中混有的乙酸
C.①、④的反应类型均属于取代反应
D.N的化学式为CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ(本题9分)乙酸乙酯是重要的工业原料和溶剂,通常混有少许乙醇和乙酸。某学习小组利用图1装置制取乙酸乙酯粗产品,再分析乙酸乙酯的含量。
| 乙酸乙酯 | 乙醇 | 乙酸 | |
| 沸点 | 77.1℃ | 78.5℃ | 117.9℃ |
操作步骤如下:
(I)准确称量20.0g乙酸乙酯粗品于锥形瓶中,用0.50mol·L—1NaOH滴定(酚酞做指示剂)。终点时消耗NaOH溶液的体积为40.0mL
(II)另取20.0g乙酸乙酯粗产品于250mL锥形瓶中,加入100mL 2.1mol·L—1NaOH溶液混合均匀后,装上冷凝箱,在水浴上加热回流约1小时,装置如图2所示。待冷却后,用0.50mol·L—1HCl滴定过量的NaOH。终点时消耗盐酸的体积为20.0mL。
回答下列问题:
(1)实验(II)中冷水从冷水凝管的 (填a或b)管口通入。
(2)利用实验(I)、(II)测量的数据计算粗产物中乙酸乙酯的质量分数为 。
(3)实验结束后,同学们对粗产品中乙酸乙酯的含量不高进行讨论。
①有人认为是实验(II)带来的误差。建议将图2中的锥形瓶改为三颈瓶,装置如图3,在三颈瓶的c、d口装配相关的仪器并进行恰当的操作,可以提高测定的精确度。你认为在三颈瓶的c、d口装配相关的仪器或操作是: (填字母);
A.装上温度计,严格控制反应温度
B.实验中经常打开瓶口,用玻璃进行搅拌
C.在反应后期,用事先安装的分液漏斗添加一定量的NaOH溶液
②还有同学认为改进乙酸乙酯的制取装置(图1)才能提高产率。拟出你的一条改进建议
Ⅱ(本题6分)如图是配制50 mL酸性KMnO4标准溶液的过程示意图。
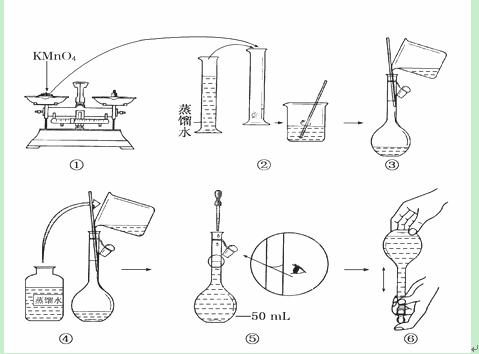
(1)请你观察图示判断其中不正确的操作有________(填序号)。
(2)其中确定50 mL溶液体积的容器是____________________________________(填名称)。
(3)如果按照图示的操作所配制的溶液进行实验,在其他操作均正确的情况下,所测得的实验结果将________(填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
阿伏加德罗常数约为6.02×1023mol-1,下列说法中正确的是
A、1.0L 1.0mol·L-1CH3COOH溶液中,CH3COOH分子数为6.02×1023
B、 Na与H2O反应生成1.12L H2(标准状况),反应中转移的电子数为6.02×1023
C、32 g S8单质中含有的S—S键个数为6.02×1023 
D、22.4 L N2中所含的分子数为6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com