
将一小块金属钠分别投入盛有:a.水、b.乙醇、c.稀H2SO4的三个小烧杯中,反应速率由快到慢的顺序为______________。解释反应速率不同的原因:________________。
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
求下列常温条件下溶液的pH(已知lg1.3=0.1,lg2=0.3,混合溶液忽略体积的变化)。
(1)0.005 mol·L-1的H2SO4溶液
(2)0.1 mol·L-1的CH3COOH溶液(已知CH3COOH的电离常数Ka=1.8×10-5)
(3)0.1 mol·L-1NH3·H2O溶液(NH3·H2O的电离度为α=1%,电离度=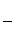 ×100%)
×100%)
(4)将pH=8的NaOH与pH=10的NaOH溶液等体积混合
(5)常温下,将pH=5的盐酸与pH=9的NaOH溶液以体积比11∶9混合
(6)将pH=3的HCl与pH=3的H2SO4等体积混合
(7)0.001 mol·L-1的NaOH溶液
(8)pH=2的盐酸与等体积的水混合
(9)pH=2的盐酸加水稀释到1 000倍
查看答案和解析>>
科目:高中化学 来源: 题型:
锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。
回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为________________(用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式:________________________________________________________________________________________________________________________________________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是________________。
①硫酸铝和氢氧化钠 ②硫酸铝和氨水 ③硫酸锌和氢氧化钠 ④硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式:________________________________________________________________________________________________________________________________________________。
试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因:_____________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构简式如图所示。下列叙述正确的是 ( )。
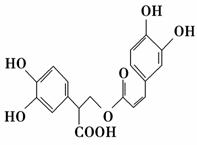
A.迷迭香酸与溴单质只能发生取代反应
B.1 mol迷迭香酸最多能和9 mol氢气发生加成反应
C.迷迭香酸可以发生水解反应、取代反应和酯化反应
D.1 mol迷迭香酸最多能与5 mol NaOH发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A(C11H8O4)在氢氧化钠溶液中加热反应后再酸化可得到化合物B和C。
回答下列问题:
(1)B的分子式为C2H4O2,分子中只有一个官能团。则B的结构简式是________,B与乙醇在浓硫酸催化下加热反应生成D,该反应的化学方程式是________________________________________________________________________。
该反应的类型是________;写出两种能发生银镜反应的B的同分异构体的结构简式________________________________________________________________________;
(2)C是芳香化合物,相对分子质量为180。其碳的质量分数为60.0%,氢的质量分数为4.4%,其余为氧,则C的分子式是________;
(3)已知C的芳环上有三个取代基。其中一个取代基无支链,且含有能使溴的四氯化碳溶液褪色的官能团及能与碳酸氢钠溶液反应放出气体的官能团,则该取代基上的官能团名称是________;另外两个取代基相同,分别位于该取代基的邻位和对位,则C的结构简式是________________________________________________________________________。
(4)A的结构简式是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)Na2O2与Na2O中均只存在离子键( )
(2)Na2O2与Na2O晶体中阳离子与阴离子的个数比均为2∶1( )
(3)2Na2O2+2H2O===4NaOH+O2↑
H2O既不是氧化剂也不是还原剂( )
(4)Na2O、Na2O2组成元素相同,与CO2反应产物也相同( )
(5)Na2O2的电子式为Na
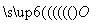 ·
· ·
·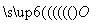
 Na( )
Na( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4NA(2014·江苏,6D)
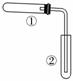
B.用如图装置进行实验,由②中澄清石灰水变浑浊,可证明①中NaHCO3固体受热分解(2014·北京理综,11C)
C.2Na2O2+2H2O===4NaOH+O2↑,是水作还原剂的氧化还原反应(2014·山东理综,7D改编)
D.过氧化钠会因为空气中的氧气而易变质(2014·上海,2A改编)
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的分离、提纯是中学化学的重要操作,请应用物质分离、提纯知识,分离下列各组混合物。
| 混合物 | 分离方法 | 操作过程 | |
| 1 | 从草木灰中提取可溶性物质 | ||
| 2 | KNO3和NaCl混合物 | ||
| 3 | 乙酸乙酯和乙酸混合物中分离乙酸乙酯 | ||
| 4 | 由乙醇溶液制无水乙醇 | ||
| 5 | 除去淀粉溶液中的碘化钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com