
分析 (1)食物的酸碱性并非指味觉上的酸碱性,也不是指化学上所指的溶液的酸碱性,而是指食物在体内代谢最终产物的性质来分类;
(2)合金是指由一种金属与其它金属或非金属熔合而成的具有金属特性的物质,金属大规模被使用的先后顺序跟金属的活动性关系最大,金属活动性较弱时,比较难形成化合物,常以单质形式存在,比较容易被利用;目前使用量最大的合金是铁合金.
解答 解:(1)苹果、菠菜含钾、钠、钙、镁等元素,在人体内代谢后生成碱性物质,属于碱性食物;鸡肉、牛奶含有较多的非金属元素,如磷、硫、氯等,在人体内氧化后,生成带有阴离子的酸根,属于酸性食物,故答案为:AD;
(2)金属大规模被使用的先后顺序跟金属的活动性关系最大,金属活动性较弱时,比较难形成化合物,常以单质形式存在,比较容易被利用,铜的活泼性较弱,比较容易冶炼,所以人类最早使用的合金材料是铜合金,目前使用量最大的合金是铁合金;
故选:C;A.
点评 本题考查了食物的酸碱性判断以及合金等,难度不大,注意食物的酸碱性是根据食物在体内代谢最终产物的性质来分类的,不是根据口感来进行分类的.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:解答题
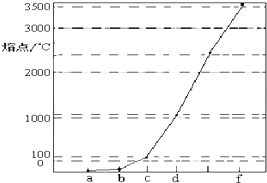
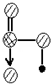 请简要说明该物质易溶于水的原因
请简要说明该物质易溶于水的原因查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 甲~庚元素在周期表中的相对位置如图,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
甲~庚元素在周期表中的相对位置如图,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )| A. | 丙与戊的原子序数相差27 | |
| B. | 气态氢化物的稳定性:庚<己<戊 | |
| C. | 丁的最高价氧化物可用于制造光导纤维 | |
| D. | 常温下,甲和乙的单质均能与水剧烈反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由水电离出的c(H+)=10-12 mol•L-1的溶液中:Na+、Cl-、HCO3-、SO42- | |
| B. | pH=12的澄清的溶液中:K+、Na+、MnO4-、SO42- | |
| C. | 甲基橙呈红色的溶液中:NH4+、Ba2+、AlO2-、Cl- | |
| D. | 加入少量铝粉后能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,22.4 L 氧气所含的分子数目为NA | |
| B. | 44 g 二氧化碳所含的原子数目为NA | |
| C. | 18 g 水所含的电子数目为9 NA | |
| D. | 1 mol 钠作为还原剂所提供的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、CO32-、NO3- | B. | Ca2+、CO32-、Na+、NO3- | ||
| C. | Na+、H+、NO3-、CO32- | D. | K+、Fe3+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用风能发电、采取节能技术、使用太阳能热水器均有利于减少二氧化碳排放 | |
| B. | 生活垃圾焚烧发电也会产生有毒有害物质 | |
| C. | 丁达尔现象可用于区别溶液与胶体,云、雾、淀粉溶液均能产生丁达尔现象 | |
| D. | 硅酸钠溶液的保存和碱溶液一样,存放在橡胶塞密封的广口试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4 L的CO气体与l mol N2所含的电子数为14 NA | |
| B. | 物质的量浓度为0.5 mol/L Mg Cl2溶液,含有Cl-数为NA | |
| C. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2 NA | |
| D. | 在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移电子数为4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com