
 室温下,把SiO2超细粉置入蒸馏水中,不断搅拌至平衡,形成 H4SiO4溶液,反应原理如下:SiO2(s)+2H2O(l)?H4SiO4(aq)△H.
室温下,把SiO2超细粉置入蒸馏水中,不断搅拌至平衡,形成 H4SiO4溶液,反应原理如下:SiO2(s)+2H2O(l)?H4SiO4(aq)△H.| 20-0.05×28-11.4 |
| 60 |
| (0.05+0.12)mol |
| 1L |


 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:
| A、人造刚玉熔点很高,可用作高级耐火材料,主要成分是二氧化硅 |
| B、化学家用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐 |
| C、提前建成的三峡大坝使用了大量水泥,水泥是硅酸盐材料 |
| D、夏天到了,游客佩戴由添加氧化亚铜的二氧化硅玻璃制作的变色眼睛来保护眼睛 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,相对分子质量为116的芳香烃A有如图的转化关系:
,相对分子质量为116的芳香烃A有如图的转化关系: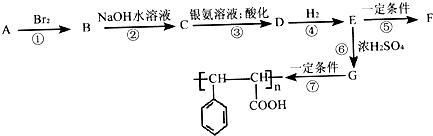
查看答案和解析>>
科目:高中化学 来源: 题型:
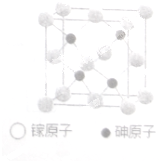 砷化稼晶体广泛用于太阳能电池、新型光源LED和通讯领域.
砷化稼晶体广泛用于太阳能电池、新型光源LED和通讯领域.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、R原子最外层电子数为5 |
| B、单质的氧化性:甲>乙 |
| C、原子半径:R>Z |
| D、HRO3与HZ的计量数比为5:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| NaOH/H2O |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 烧杯中通入过量的CO2,出现白色沉淀,则溶液中一定含有AlO2- 烧杯中通入过量的CO2,出现白色沉淀,则溶液中一定含有AlO2- |
B、 装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、氧化性 装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、氧化性 |
C、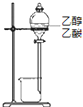 装置可以除去乙醇中的乙酸 装置可以除去乙醇中的乙酸 |
D、 装置可以比较碳酸钠、碳酸氢钠的热稳定性 装置可以比较碳酸钠、碳酸氢钠的热稳定性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com