
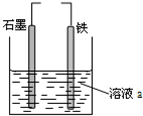
| A. | 若两电极直接连接,a是食盐水,则发生析氢腐蚀 | |
| B. | 若铁接电源负极,石墨接电源正极,a是稀H2SO4溶液,电解一段时间后溶液的pH增大 | |
| C. | 若两电极直接连接,则电子从铁流向石墨 | |
| D. | 若铁接电源正极,石墨接电源负极,a是氯化铜溶液,阴离子向石墨电极移动 |
分析 A、在中性环境下,金属会发生吸氧腐蚀;
B、电解硫酸溶液的实质是电解水,水量减少,酸的浓度增加;
C、电解池中,电子从阳极沿着导线流向阴极;
D、电解池中,电解质的阴离子移向阳极,阳离子移向阴极.
解答 解:A、若两电极直接连接,a是食盐水,则发生吸氧腐蚀,故A错误;
B、若铁接电源负极,石墨接电源正极,a是稀H2SO4溶液,实际上是电解水,电解一段时间后溶液浓度增大,pH减小,故B错误;
C、若两电极直接连接则铁作负极,电子由铁流向石墨,故C正确;
D、阴离子向阳极移动,故阴离子向铁电极移动,故D错误,
故选C.
点评 本题考查学生金属的腐蚀以及电解池、原电池的工作原理知识,注意知识的梳理和归纳是解题的关键,难度不大.


科目:高中化学 来源: 题型:推断题
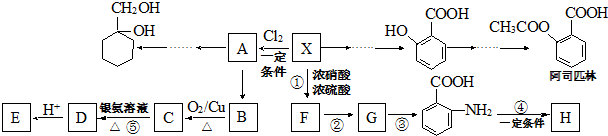
 (苯胺,易被氧化)
(苯胺,易被氧化)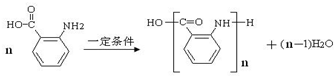 .
.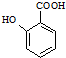 的同系物M比其本身相对分子质量大14,M的同分异构体中能同时满足以下条件:①芳香族化合物,②能发生水解反应,③与FeCl3溶液能够发生显色反应;共有19(不考虑立体异构)种.
的同系物M比其本身相对分子质量大14,M的同分异构体中能同时满足以下条件:①芳香族化合物,②能发生水解反应,③与FeCl3溶液能够发生显色反应;共有19(不考虑立体异构)种.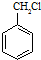 和其他无机物合成
和其他无机物合成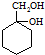 最合理的方案.
最合理的方案.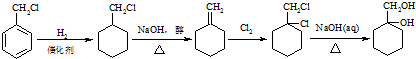 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
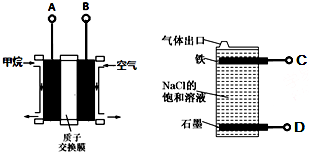
| A. | 燃料电池的A极连接电解池的C极 | |
| B. | 燃料电池工作时当0.2 NA个H+通过质子交换膜移向右边,饱和食盐水中可产生2.24L气体 | |
| C. | A电极的电极反应式为:CH4-8e-+2H2O═CO2+8H+ | |
| D. | 电解池总反应式为NaCl+H2O$\frac{\underline{\;电解\;}}{\;}$NaClO+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
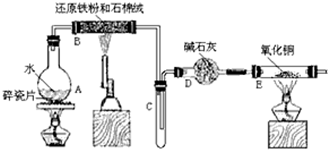
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水使有色布条褪色 | B. | 过氧化钠使某些染料褪色 | ||
| C. | 二氧化硫使品红溶液褪色 | D. | 活性炭使红墨水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
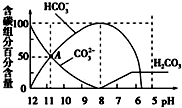
| A. | 0.1 mol/L Na2CO3溶液中c(Na+)+c(H+)═2c(CO32-)+c(HCO3-)+c(OH-) | |
| B. | 当加入20 mL盐酸时,混合溶液的pH约为8 | |
| C. | 常温下CO2饱和溶液的pH约为5.6 | |
| D. | 在A点:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com