
【题目】化学与生产、生活密切相关,下列表述错误的是( )
A.使用新能源,减少化石燃料的燃烧,可防止酸雨的产生
B.明矾在水中能形成胶体,可作为净水剂
C.建设三峡大坝使用了大量水泥,水泥是硅酸盐材料
D.给汽车安装尾气转化装置,易产生光化学烟雾
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】中国沿海某城市采用反渗透法将海水淡化,得到淡水供市民使用,剩余母液继续加工获得其他产品。母液中主要含有Cl-、Na+、K+、Mg2+ 、Ca2+、SO42-、Br-等离子。某实验小组同学模拟工业生产流程,进行如下实验.

(1)写出实验室制备氯气的化学方程式_____________________;
(2)海水淡化的方法还有____________(写出一种);
(3)I中,电解饱和食盐水的工业生产叫做氯碱工业,写出该反应的离子方程式______;
(4)Cl2和Br2均为双原子分子,从原子结构的角度解释其原因_____________________;
(5)Ⅲ中,加入适量CaCl2固体的目的是_____________________;
(6)写出IV中反应的离子方程式_____________________;
(7)与过程II类似,工业上常用“空气吹出法”实现海水提溴,将1m3海水浓缩至1L,使用该法最终得到36g Br2,若提取率为60%,则原海水中溴的浓度为_________ mg/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)同温同压下的两个相同容器中分别装有O2和O3气体,则两瓶气体中分子数之比是______,原子数之比是______,质量之比是______,密度之比是______
(2)下列所给出的几组物质中:含有分子数最多的是_________;含有原子数最多的是_________;标准状况下体积最大的是____________。
① 1gH2; ② 2.408×1023个CH4 ;③ 10.8gH2O; ④ 标准状况下6.72LCO2
(3)设NA表示阿伏加德罗常数,如果ag某气体含有的分子数是b,则cg该气体在标准状况下的体积是_________________(用含NA的式子表示)。
(4)配制100 mL 1mol/L的的稀H2SO4溶液,需要用量筒量取质量分数为98%的浓H2SO4(密度为1.84g/cm3)的体积为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可以直接氧化PCl3制备POCl3。某兴趣小组模拟该工艺设计实验装置如下(某些夹持装置、加热装置已略去):

部分物质的性质如下表:
熔点/℃ | 沸点/℃ | 其他 | |
PCl3 | -112 | 75.5 | 遇水生成H3PO3和HCl,遇O2生成POCl3,缓慢通入氧气POCl3产率较高 |
POCl3 | 2 | 105.3 | 遇水生成H3PO4和HCl,能溶于PCl3 |
实验步骤如下
I.连接仪器,检查装置气密性。关闭K1、K2 打开K3、K4,点燃酒精灯制备气体。
II.缓慢向C中通入适量气体至C中白磷消失,熄灭酒精灯。
III.关闭K3、K4,打开K1、K2 ,A中开始发生反应。
IV.C装置控制反应在60℃~65℃,最终制得POCl3产品。
回答下列问题:
(1)B、D装置中盛放的试剂是_______,B装置的作用除了干燥O2和平衡气压之外,还有___。
(2)仪器a的名称是______,装置E 中发生反应的离子方程式为____________。
(3)步骤IV 控制温度60℃~65℃,其主要目的是____________。
(4)该实验装置存在一处明显的设计缺陷是_______________。
(5)通过下面步骤可以测定三氯氧磷产品中Cl 的含量:
I.取xg产品于锥形瓶中,加入足量NaOH 溶液,PCl3完全反应后加稀硝酸至酸性。
II.向锥形瓶中加入0.1000mol/L 的AgNO3溶液40.00 mL,使Cl-完全沉淀。
III.向其中加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖。
IV.加入指示剂,用cmol/LNH4SCN溶液滴定过量Ag+至终点,记下所用体积VmL。
(己知: Ag3PO4溶于酸,Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10 -12)
①滴定选用的指示剂是_____(填标号)
a.酚酞 b.淀粉 c.NH4Fe(SO4)2 d.甲基橙
②元素Cl的质量分数为(列出算式)________________。
③步骤III若不加入硝基苯,所测Cl含量将会_______(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如右,电解总反应为:2Cu+H2O![]() Cu2O+H2↑。下列说法正确的是
Cu2O+H2↑。下列说法正确的是
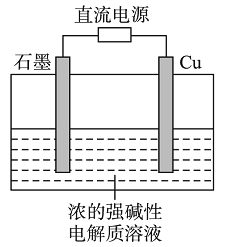
A. 石墨电极上产生氢气
B. 铜电极发生还原反应
C. 铜电极接直流电源的负极
D. 当有0.1 mol电子转移时,有0.1 mol Cu2O生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】强酸和强碱的稀溶液中和时,中和热为57.3kJ,试计算:
(1)浓度为0.1mol·L-1的NaOH溶液200mL,与足量酸反应时,能放出多少千焦的热量_____?
(2)浓度为5%的H2SO4溶液980g,与足量的NaOH溶液反应,能放出多少热量______ ?
(3)用浓度为0.2mol·L-1的HNO3 100mL,与足量的NaOH溶液反应,能放出多少热量_____ ?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com