
分析 ①向氨水中加入氯化镁固体时,镁离子和氢氧根离子反应生成氢氧化镁沉淀,促进一水合氨电离;
②加入浓盐酸,氢离子和氢氧根离子反应生成水,从而促进一水合氨电离.
解答 解:①向氨水中加入氯化镁固体时,镁离子和氢氧根离子反应生成氢氧化镁沉淀,氢氧根离子浓度减小,促进一水合氨电离,则溶液中铵根离子浓度增大,
故答案为:正反应;减少;增大;
②加入浓盐酸,氢离子和氢氧根离子反应生成水,从而促进一水合氨电离,则溶液中氢氧根离子浓度减小,铵根离子浓度增大,温度不变,水的离子积常数不变,则氢离子浓度增大,
故答案为:正反应;NH4+、H+.
点评 本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,再结合溶液中离子浓度变化确定平衡移动方向,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ③或④ | C. | ①或③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应在0~10 s内,用Z表示的反应速率为0.158 mol•L-1•s-1 | |
| B. | 反应在0~10 s内,X的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应进行到10 s时,Y的转化率为79.0% | |
| D. | 反应的化学方程式为X(g)+Y(g)═Z(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
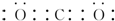
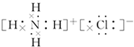

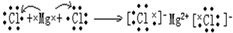 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,1 L 0.1 mol•L-1 NH4NO3溶液中的氮原子数为0.2NA | |
| B. | 含有58.5 g氯化钠的溶液中含有NA个氯化钠分子 | |
| C. | 在反应KIO3+6HI═KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA | |
| D. | 常温常压下,22.4 L乙烯中C-H的个数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L HA(某酸)溶液pH≠1,0.1 mol/L BOH(某碱)溶液中c(OH-)=0.1 mol/L,则BA(盐)溶液pH<7 | |
| B. | pH=2的盐酸与pH=l的硫酸溶液中c(H+)之比为2:1 | |
| C. | pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则c (Na+)+c(H+)=c(OH-)+c(CH3COO-) | |
| D. | 4种pH相同的溶液①CH3COONa ②NaHCO3 ③NaOH中c(Na+)的大小顺序是②>①>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 |
| ①取少量甲溶液,滴加几滴甲基橙 | 溶液变红色 |
| ②取少量甲溶液,滴加Ba(NO3)2溶液 | 溶液无明显变化 |
| ③取②中实验后的溶液,滴加AgNO3溶液 | 有白色沉淀生成,且不溶于HNO3 |
| ④取少量甲溶液,滴加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com