
 | 1 | 2 | 3 | 4 |
| V( 样品 ) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(初读数) | 0.00 | 0.50 | 0.70 | 1.00 |
| V(NaOH)(终读数) | 22.60 | 22.25 | 22.05 | 23.00 |
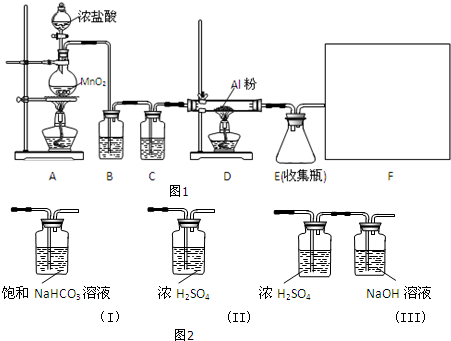
分析 浓盐酸和二氧化锰反应生成氯气,B中的饱和食盐水是为了除去混有的HCl气体,C中的浓硫酸是为了除去水,氯气与铝反应生成氯化铝,因为氯化铝易发生水解,故F应该防止空气中的水蒸气进入E装置和吸收尾气.
(1)根据浓盐酸和二氧化锰的性质判断生成物,从而确定方程式;
(2)B中的饱和食盐水是为了除去混有的HCl气体;
(3)F应该防止空气中的水蒸气进入E装置和吸收尾气;
(4)AlCl3遇水水解生成氢氧化铝和氯化氢;
(5)①先求出氢氧化钠的平均体积,由CHClVHCl=CNaOHVNaOH解题;
②根据c(待)=$\frac{c(标)×V(标)}{V(待)}$判断不当操作对相关物理量的影响;
(6)A.化合价升高得到的是氧化产物;
B.氯化氢和氯化铝不电离;
C.Al2O3+3C+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2AlCl3+3CO,碳总共失去6mol电子;
D.一氧化碳和COCl2有毒.
解答 解:(1)浓盐酸和二氧化锰在加热条件下能发生氧化还原反应生成氯化锰、氯气、水:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)B中的饱和食盐水是为了除去混有的HCl气体,故答案为:除去Cl2中混有的HCl气体;
(3)F应该防止空气中的水蒸气进入E装置和吸收尾气,应选III,故答案为:III;
(4)AlCl3遇水水解生成氢氧化铝和氯化氢,离子方程式:Al3++3H2O?Al(OH)3+3H+,故答案为:AlCl3遇水水解,Al3++3H2O?Al(OH)3+3H+,产生的氯化氢气体在空气中形成酸雾;
(5)①反应消耗的V(NaOH)分别为22.60,22.25-0.5=21.75,22.05-0.7=21.35,23.00-1.00=22.00
平均为$\frac{22.60+21.75+21.35+22}{4}$=22.00mL
该次滴定测得试样中盐酸浓度为,由CHClVHCl=CNaOHVNaOH可得CHCl×20=0.2000×22.00
盐酸的浓度为0.2200mol/L,故答案为:0.2200;
②a.开始滴定时滴定管尖嘴处留有气泡,滴定结束气泡消失,标准液题体积偏大,实验结果偏大;
b.未用标准NaOH溶液润洗滴定管,标准液的浓度偏小,体积偏大,实验结果偏大;
c.锥形瓶中加入待测盐酸后,再加少量水,实验结果无影响;
d.有少量液体溅出,溶质的物质的量减小,实验结果偏小;
e.滴定前锥形瓶用待测盐酸润洗,消耗标准液体积偏大,实验结果偏大;
f.观察读数时,滴定前仰视,滴定后俯视,读出体积偏小,实验结果偏小;
故答案为:df;
(6)A.Al2O3+3C+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2AlCl3+3CO中氯化铝是还原产物,故A错误;
B.氯化氢和氯化铝是共价化合物,不电离,不能书写离子方程式,故B错误;
C.Al2O3+3C+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2AlCl3+3CO,碳总共失去6mol电子,每产生2mol AlCl3时转移电子数为6NA,故C正确;
D.一氧化碳和COCl2有毒,会造成污染,故D正确.
故答案为:CD.
点评 本题考查了实验室制备氯气,中和滴定的实验操作,侧重实验基本操作和实验原理的考查,题目难度中等,注意把握实验设计的仪器连接顺序,清楚实验原理.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:选择题
| A. | 物质的量相同的气体单质具有相同的原子数 | |
| B. | 铁原子的摩尔质量等于它的相对原子质量 | |
| C. | 反应前各反应物的物质的量之和一定等于反应后各生成物的物质的量之和 | |
| D. | 一个氧原子的实际质量等于$\frac{16}{6.02×1{0}^{23}}$g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 S2Cl2是工业上常用的硫化剂,广泛应用于石油化工.实验室制备S2Cl2的方法有两种:
S2Cl2是工业上常用的硫化剂,广泛应用于石油化工.实验室制备S2Cl2的方法有两种:| S | CS2 | CCl4 | S2Cl2 | |
| 熔点/ | 113 | -109 | -23 | -77 |
| 沸点/ | 445 | 47 | 77 | 137 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图表示在一定的温度下,容积固定的密闭容器中,A、B、C三种气体物质的浓度随时间变化的情况,试回答下列问题:
如图表示在一定的温度下,容积固定的密闭容器中,A、B、C三种气体物质的浓度随时间变化的情况,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 (写结构简式)可以合成二肽(如图2)
(写结构简式)可以合成二肽(如图2)查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .请写出A与稀、冷的KMnO4溶液反应生成有机产物与足量醋酸反应的化学方程式为
.请写出A与稀、冷的KMnO4溶液反应生成有机产物与足量醋酸反应的化学方程式为 +2CH3COOH$→_{△}^{浓硫酸}$
+2CH3COOH$→_{△}^{浓硫酸}$ +2H2O.
+2H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com