
【题目】在密闭容器中,反应X2(g)+Y2(g)![]() 2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是( )
2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是( )
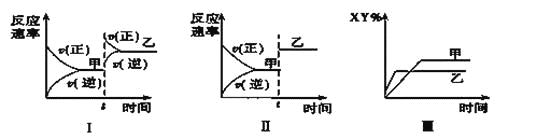
A. 图Ⅰ是增大压强的变化情况
B. 图Ⅱ是一定是加入催化剂的变化情况
C. 图Ⅲ是增大压强或升高温度的变化情况
D. 图Ⅲ一定是升高温度的变化情况
科目:高中化学 来源: 题型:
【题目】下图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量。下列反应对应的曲线不正确的是

A. 向NaA1O2溶液中滴人HC1至过量
B. 向澄清石灰水中通人CO2至过量
C. 向含有盐酸的A1C13溶液中滴人NaOH溶液至过量
D. 向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至沉淀消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关滴定操作的顺序正确的是
①检查滴定管是否漏水;②用蒸馏水洗涤玻璃仪器;③用标准溶液润洗盛装标准溶液的滴定管,用待测液润洗盛待测液的滴定管;④装标准溶液和待测液并调整液面(记录初读数);⑤取一定体积的待测液于锥形瓶中:⑥滴定操作
A. ①③②④⑤⑥ B. ①②③④⑤⑥ C. ②③①④⑤⑥ D. ④⑤①②③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见的氧化物,气体E是单质F所含元素的氢化物。
(1) A能溶于强酸、强碱,写出A与强碱溶液反应的离子方程式: ______________________________。
(2)B、D都是酸性氧化物且组成元素相同,D溶于水得强酸,则B、D分子中除氧元素外所含另一种元素在元素周期表中的位置是______________________。
(3)E能使湿润的红色石蕊试纸变蓝,实验室制取E气体的化学方程式为______________________,制得的气体可用如图所示装置收集,则气体应从______(填“A”或“B”)通入。

(4)由各分解产物的物质的量之比推测X的组成类似于明矾,若向X的浓溶液中滴加浓NaOH溶液至过量,现象依次为_______________、___________________、_______________________________。
(5)取一定量的X晶体分解,若生成1 mol F,则必同时生成 ____________(填化学式)________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:WO3 (s) + 3H2 (g) ![]() W (s) + 3H2O (g)
W (s) + 3H2O (g)
请回答下列问题:
(1)上述反应的化学平衡常数表达式为___________________________。
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为_____;随温度的升高,H2与水蒸气的体积比减小,则该反应为反应_______(填“吸热”或“放热”)。
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
温度 | 25℃ ~ 550℃ ~ 600℃ ~ 700℃ |
主要成份 | WO3 W2O5 WO2 W |
第一阶段反应的化学方程式为_____________;
580℃时,固体物质的主要成分为________;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为____________。
(4)已知:温度过高时,WO2 (s)转变为WO2 (g);
WO2 (s) + 2H2 (g) ![]() W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1
W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1
WO2 (g) + 2H2(g) ![]() W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1
W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1
则WO2 (s) ![]() WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、恒容的密闭容器中,混合气体A、B、C 的物质的量浓度(c)与时间(t) 的关系如下表所示:

请填空:
(1)前2mim内,v(B)= _________________。
(2) 到2mim末A 的转化率为____________。
(3)该反应的化学方程式为______________________________________________。
(4)6 min - 8 min若只改变了反应体系中某一种物质的浓度,则应为_______(填选项字母)
a.增大A的浓度 b.减小B的浓度 c.增大C的浓度
则该物质的浓度改变量为________________mol·L -1
(5)如果在相同条件下,若开始加入的三种物质的物质的量浓度是原来的2倍,则______是原来的2倍。
a. A的转化率 b. B的平衡浓度
c.达到平衡的时间 d.平衡时气体的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中(如图所示平面图),经过一段时间后,下列说法中正确的是

A. Ⅰ附近溶液pH降低
B. Ⅳ附近很快生成铁锈
C. Ⅲ附近产生黄绿色气体
D. Ⅱ附近很快出现蓝色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解足量的NaCl溶液一段时间后,欲使溶液恰好恢复至电解前情况,可加入的物质是
A. NaCl B. H2O C. 盐酸 D. HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com