
实验:①0.1 mol/L AgNO3溶液和0.1 mol/L NaCl溶液等体积混合得到浊液,过滤。
②分别取少量①的滤液,分别滴加等浓度等体积的饱和Na2S溶液、饱和Na2SO4溶液,前者出现浑浊,后者溶液仍澄清。
③取少量①的沉淀,滴加几滴氨水,沉淀逐渐溶解。
下列分析不正确的是
A.实验②证明了①的滤液中含有Ag+,由此推断①的滤液中也含有Cl
B.实验②证明了该温度下Ag2S比Ag2SO4更难溶解
C.实验③的溶液中含有Ag(NH3)2+微粒
D.由实验③推测:若在①的沉淀中滴加NaOH溶液,沉淀也能溶解
 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源:2014-2015学年山东省日照市高三3月模拟考试理综化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.向NH4HCO3溶液中加过量NaOH溶液并加热: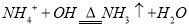
B.用KIO3氧化酸性溶液的KI: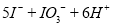 ==
==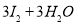
C.向Ba(OH)2溶液中滴加稀硫酸: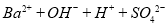 ==
==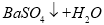
D.用稀硝酸洗涤试管内壁的银镜: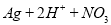 ==
==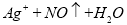
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三3月月考理综化学试卷(解析版) 题型:填空题
(13分)利用铜萃取剂M,通过如下反应实现铜离子的富集:
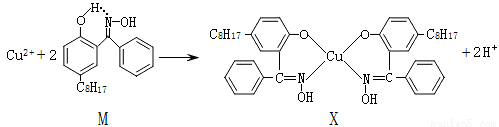
(1)X难溶于水、易溶于有机溶剂,其晶体类型为 。
(2)M所含元素的电负性由大到小顺序为 ,N原子以 轨道与O原子形成σ键。
(3)上述反应中断裂和生成的化学键有 (填序号)。
a.离子键
b.配位键
c.金属键
d.范德华力
e.共价键
(4)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是 。
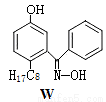
(5)基态Cu2+的外围电子排布式为 ,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。判断Sc3+、Zn2+的水合离子为无色的依据是 。
离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省福州市高三3月月考理综化学试卷(解析版) 题型:选择题
某同学为研究电化学原理,使用KC1盐桥设计如图所示实验装置。下列分析不合理的是
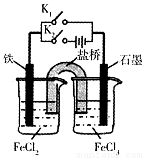
A.闭合K2断开K1,左侧烧杯中的Fe2+向铁电极移动
B.无论闭合K1断开K2,还是断开K1闭合K2,石墨电极上发生的反应都是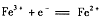
C.闭合K,断开K2,电流从石墨电极经过K.流向铁电极
D.闭合K,断开K2,左侧烧杯中的溶液pH将逐渐降低
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三上学期期末考试化学试卷(解析版) 题型:填空题
(12分)已知:2X(g)+Y(g) a Z(g),T1温度时,在体积为2L的密闭容器中充入6mol X和2 mol Y,根据图示回答:
a Z(g),T1温度时,在体积为2L的密闭容器中充入6mol X和2 mol Y,根据图示回答:

(1)a=__;用X的浓度变化表示从反应开始到平衡时的平均反应速率为 mol/(Lmin)。
(2)平衡时,Y在混合物中的物质的量分数是 。
(3)下列选项能说明反应达到平衡状态的是 (选填字母)。
A.容器内压强保持不变
B.容器内密度保持不变
C.X的物质的量不再变化
D.υ(X)正 =υ(Z)逆
(4)其他条件相同时,若升高温度到T2时,反应的平衡常数为1,下列措施可以提高Y的转化率的是 (选填字母)。
A.选择适当的催化剂 B.分离出Z
C.增大压强 D.升高温度
(5)X、Y、Z由C、H、O三种元素中的一种或几种组成,信息如下:
物质 | X | Y | Z |
所含元素种数 | 1 | 2 | 3 |
分子中的电子总数 | 大于10 | 18 | |
燃烧热(kJ/mol) | -285.8 | -283 | -726.5 |
①则Z的分子式为___________。
②根据燃烧热数据分析,等质量的X、Y、Z充分燃烧,放出热量最多的是__________(填分子式)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三上学期期末考试化学试卷(解析版) 题型:选择题
某同学组装了如图所示的原电池装置,下列叙述中正确的是

A.电流方向:电极Ⅱ→ →电极Ⅰ
→电极Ⅰ
B.电极Ⅱ逐渐溶解
C.电极Ⅰ上发生还原反应
D.盐桥中装有含氯化钾的琼脂,Cl向右池移动
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三上学期期末考试化学试卷(解析版) 题型:选择题
下列电池属于二次电池的是
|
|
|
|
A.锌银钮扣电池 | B.氢氧燃料电池 | C.铅蓄电池 | D.锌锰干电池 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省商丘市高三第一次模拟考试化学试卷(解析版) 题型:选择题
某烃有两种或两种以上的同分异构体,其某一种同分异构体的一氯代物只有一种,则这种烃可能是
①分子中含有7个碳原子的芳香烃 ②分子中含有4个碳原子的烷烃
③分子中含有12个氢原子的烷烃 ④分子中含有8个碳原子的烷烃
A.③④ B.②③ C.①② D.②④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三第一次模拟考试理科综合化学试卷(解析版) 题型:实验题
(20分)下图是在实验室进行氨气快速制备与性质实验的组合装置,部分固定装置未画出。
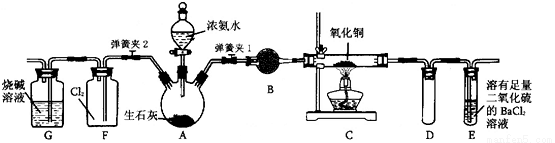
(1)在组装好装置后,若要检验A~E装置的气密性,其操作是首先____,然后微热A,观察到E中有气泡冒出,移开酒精灯或松开双手,E中导管有水柱形成,说明装置气密性良好。
(2)装置B中盛放的试剂是________。
(3)点燃C处酒精灯,关闭弹簧夹2,打开弹簧夹l,从分液漏斗放出浓氨水至浸没烧瓶中固体后关闭分液漏斗,稍候片刻,装置C中黑色固体逐渐变红,装置E中溶液里出现大量气泡,同时还可能产生的现象是________;从E中逸出液面的气体可以直接排入空气,请写出在C中发生反应的化学方程式:________。
(4)当C中固体全部变红色后,关闭弹簧夹1,慢慢移开酒精灯,待冷却后,称量C中固体质量,若反应前固体质量为16 g,反应后称重固体质量减少2.4 g,通过计算确定该固体产物的成分是________(用化学式表示)。
(5)在关闭弹簧夹1后,打开弹簧夹2,残余气体进入F中,很快发现装置F中产生白烟,同时发现G中溶液迅速倒吸流入F中。请写出产生白烟的化学方程式:________,迅速产生倒吸的原因是________。
(6)为了汪明一水合氨是弱碱,甲、乙两同学分别设计以下实验进行探究。
①甲同学用pH试纸测得室温下0.l mol/L氨水pH为10,则认定一水合氨是弱电解质,理由是________。
②乙同学取出10 mL 0.1 mol/L氨水,滴入2滴酚酞试液,显粉红色,再加入NH4Cl晶体少量,观察到的现象是________,则证明一水台氨是弱电解质。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com