
| A. | 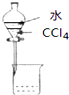 分离水和CCl4 | B. | 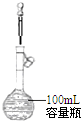 定容 | ||
| C. | 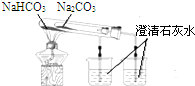 比较两种盐的热稳定性 | D. | 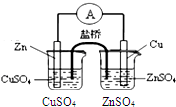 构成铜锌原电池 |
分析 本题考查的实验操作的分析与评价,涉及分液操作,配制溶液时容量瓶的定容,套管实验分析碳酸钠与碳酸氢钠的稳定性,要求间接加热碳酸氢钠固体,铜锌原电池,要求正极和负极池内分别发生还原反应和氧化反应;
A.水和CCl4分层,水在上层;
B.加水至刻度线1~2cm处改用胶头滴管定容;
C.碳酸氢钠不稳定,加热易分解;
D.盐桥的作用是平衡两个半电池中的阴阳离子,使该装置构成闭合回路,断开后两池都不再发生反应.
解答 解:A.水和CCl4分层,水在上层,可利用分液漏斗分离,故A正确;
B.加水至刻度线1~2cm处改用胶头滴管定容,则加水太少,还不能定容,故B错误;
C.碳酸氢钠不稳定,加热易分解,则为了对比性,应在温度低的小试管中加碳酸氢钠,故C错误;
D.该装置中发生的电池反应是锌和铜离子的置换反应,该原电池中,锌的活泼性大于铜,所以锌作负极,铜作正极;正极上铜离子得电子发生还原反应,电极反应式为:Cu2++2e-=Cu;负极上锌失电子生成锌离子进入溶液,所以锌片逐渐溶解;外电路中,电子从负极锌沿导线流向正极铜;盐桥中的阴离子向硫酸锌溶液中迁移,阳离子向硫酸铜溶液中迁移,而图中锌插在硫酸铜溶液中,铜插在硫酸锌溶液中,假设锌能失去电子,沿导线进入铜极,因盐桥作用是平衡两个半电池中的阴阳离子,只有盐桥中的阴阳离子移动,所以左图中的硫酸铜中的铜离子无法得电子,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物的分离提纯、溶液配制、稳定性比较等,把握实验技能、实验原理及实验装置为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr
+HBr查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 $→_{85℃}^{浓H_{2}SO_{4}}$
$→_{85℃}^{浓H_{2}SO_{4}}$

| 密度(g•cm-3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A. | 反应在前5s的平均速率v(A)=0.17mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(A)=0.41mol•L-1,则反应的△H>0 | |
| C. | 相同温度下,起始时向容器中充入2.0mol C,达到平衡时,C的转化率大于80% | |
| D. | 相同温度下,起始时向容器中充入0.20mol A、0.20mol B和1.0mol C,反应达到平衡前v(正)<v(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度只能加快吸热反应速率 | |
| B. | 对于任何反应,增大压强都可加快反应速率 | |
| C. | 使用正催化剂只加快正反应速率 | |
| D. | 催化剂可以改变反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com