
为了预防碘缺乏病,国家规定每千克食盐中应含有40—50 mg的碘酸钾。为检验某种食盐是否为加碘的合格食盐,某同学取食盐样品428 g,设法溶解出其中全部的碘酸钾,将溶液酸化并加入足量的碘化钾淀粉溶液,溶液呈蓝色,再用0.030 mol·L-1的硫代硫酸钠溶液滴定,用去18.00 mL时蓝色刚好褪去。试通过计算说明该加碘食盐是否为合格产品。
有关反应如下:![]() +5I-+6H+====3I2+3H2O,I2+2
+5I-+6H+====3I2+3H2O,I2+2![]() ====2I-+
====2I-+![]()
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| H2O2,H+ |
| 70℃ |
| K2CO3 |
| 滴定次数 | 盛标准Na2S2O4溶液的读数 | |
| 滴定前刻度(/mL) | 滴定后刻度(/mL) | |
| 1 | 1.02 | 11.03 |
| 2 | 2.00 | 11.99 |
| 3 | 0.20 | 10.20 |
| 1270 |
| 3w |
| 1270 |
| 3w |
查看答案和解析>>
科目:高中化学 来源: 题型:
![]() +5I-+6H+
+5I-+6H+![]() 3I2+3H2O
3I2+3H2O
I2+![]()
![]() 2I-+
2I-+![]()
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省嘉兴一中高二上学期期中考试化学试卷 题型:计算题
(5分)为了预防碘缺乏病,国家规定每千克食盐中应含有18~50毫克的碘元素。为检验某种食盐是否为加碘的合格食盐,某同学取食盐样品500克,设法溶解出其中全部的碘酸钾。将溶液酸化并加入足量的碘化钾淀粉溶液,溶液呈蓝色,再用0.01mol/L的硫代硫酸钠(Na2S2O3)溶液滴定,用去10.00mL时蓝色刚好褪去。用双线桥法标注①的电子转移情况并通过计算说明该加碘食盐是否为合格产品。
(有关反应:①IO3-+5I-+6 H+==3I2+3H2O ②I2+2Na2S2O3="=2" NaI+Na2S4O6)
查看答案和解析>>
科目:高中化学 来源:2011届浙江省海盐元济高级中学高三高考全真压轴考试(理综)化学试题 题型:实验题
为了预防碘缺乏病,有关部门规定食盐中的碘含量(以I计)应在20~50 mg/Kg。制备KIO3的方法如下:
方法1:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑;KH(IO3)2+KOH=2KIO3+H2O
方法2:碱性条件下,
方法3: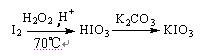
⑴与方法3相比方法1的不足是 ,方法2的不足是 。
⑵方法2选用的电极是惰性电极,则其阳极反应式是 。
⑶方法3反应温度控制在70℃左右,不采用更高温度的主要原因是 。
⑷制备纯净KIO3的实验步骤中,最后需将所得晶体最好使用 洗涤2~3次,干燥后得产品。
⑸已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O; I2+2S2O32-=2I-+S4O62-。为测定加碘食盐中碘的含量,设计的方案如下。请完善实验步骤并计算测定结果:
I2+2S2O32-=2I-+S4O62-。为测定加碘食盐中碘的含量,设计的方案如下。请完善实验步骤并计算测定结果:
a.准确称取w g食盐于锥形瓶中,再加适量蒸馏水使其完全溶解。
b. 。
c.向锥形瓶中滴加2.0×10-3 mol/L Na2S2O3标准溶液至终点。
d.重复上述实验两次。
三次实验的数据记录如下表。则所测加碘食盐样品中的碘元素含量是 mg/kg(以含w的代数式表示)。
| 滴定次数 | 盛标准Na2S2O3溶液的读数 | |
| 滴定前刻度(/mL) | 滴定后刻度(/mL) | |
| 1 | 1.02 | 11.03 |
| 2 | 2.00 | 11.99 |
| 3 | 0.20 | 10.20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com