
【题目】高分子材料M在光聚合物和金属涂料方面有重要用途,M的结构简式为:

工业上合成M的过程可表示如下:

已知:A完全燃烧只生成CO2和H2O,其蒸汽密度是相同状况下氢气密度的43倍,分子中H、O原子个数比为3∶1,它与Na或Na2CO3都能反应产生无色气体。
(1)A中官能团的名称是羧基、_________。
(2)下列说法正确的是_________(填字母)。
a.工业上,B主要通过石油的裂解获得
b.C的同分异构体有3种(不包括C)
c.E―→M的反应是加聚反应
(3)写出反应A+D+H3PO4―→E的化学方程式:_________,该反应类型是_________反应。
(4)F是A的一种同分异构体,F的核磁共振氢谱显示分子中有两种不同的氢原子。存在下列转化关系:

写出F、N的结构简式:F_________;N_________。写出反应①的化学方程式_______。
【答案】碳碳双键 abc 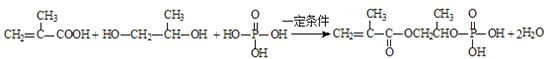 酯化(取代)
酯化(取代) ![]()
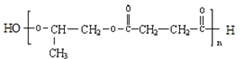
![]()
【解析】
B的分子式为:C3H6,能与![]() 的
的![]() 溶液发生加成反应,则B的结构简式为:
溶液发生加成反应,则B的结构简式为:![]() ,C的结构简式为:
,C的结构简式为:![]() ,D的结构简式为:
,D的结构简式为:![]() ,A完全燃烧只生成CO2和H2O,A的蒸气密度是相同状况下氢气密度的43倍,可知A的相对原子质量为:
,A完全燃烧只生成CO2和H2O,A的蒸气密度是相同状况下氢气密度的43倍,可知A的相对原子质量为:![]() ,分子中
,分子中![]() 、
、![]() 原子个数比为3:1,且与Na或Na2CO3都能反应产生无色气体,说明分子中含有羧基(
原子个数比为3:1,且与Na或Na2CO3都能反应产生无色气体,说明分子中含有羧基(![]() ),D与A、
),D与A、![]() 反应得到E,E转化得到M,结合M的结构简式可知,A的结构式简式为:
反应得到E,E转化得到M,结合M的结构简式可知,A的结构式简式为:![]() ,E的结构简式为:
,E的结构简式为: 。
。
(1)由上述分析可知,A的结构简式为:![]() ,含有官能团为:碳碳双键、羧基;
,含有官能团为:碳碳双键、羧基;
(2)a. B的结构简式为:CH3CH=CH2,通过石油的裂解获得,a正确;
b. C的结构简式为:CH2BrCHBrCH3,对应的同分异构体有CHBr2CH2CH3、CH3CBr2CH3、CH2BrCH2CH2Br,不包括C有3种,b正确;
c. ![]() 的反应是加聚反应,c正确。
的反应是加聚反应,c正确。
(3)![]() 的化学反应方程式为:
的化学反应方程式为:

该反应类型:酯化反应(取代反应);
(4)F是A的一种同分异构体,F的核磁共振氢谱显示分子中有两种不同的氢原子,且能与新制氧化铜发生氧化反应可知,F分子中含有![]() ,其结构简式为:
,其结构简式为:![]() ,被氧化生成H,H的结构简式为:
,被氧化生成H,H的结构简式为:![]() ,H与D发生缩聚反应生成N,N的结构简式为:
,H与D发生缩聚反应生成N,N的结构简式为: ,反应①的化学反应方程式为:
,反应①的化学反应方程式为:
![]()


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】常温下,向20.00 mL 0.100 mol·L-1 CH3COONa溶液中逐滴加入0.100 0 mol·L-1盐酸,溶液的pH与所加盐酸体积的关系如下图所示(不考虑挥发)。下列说法正确的是
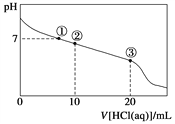
A. 点①所示溶液中:c(CH3COOH)=c(Cl-)>c(OH-)=c(H+)
B. 点②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH)
C. 点③所示溶液中:c(CH3COOH)>c(Na+)>c(H+)>c(CH3COO-)
D. 整个过程中可能出现:c(H+)+c(Na+)=c(CH3COOH)+c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同条件下,用O2氧化a mol/L FeCl2溶液过程中所测的实验数据如图所示。下列分析或推测合理的是

A. 由①、②可知, pH越大,+2价铁越易被氧化
B. 由②、③推测,若pH>7,+2价铁更难被氧化
C. 由①、③推测,FeCl2被O2氧化的反应为放热反应
D. 60℃、pH=2.5时, 4 h内Fe2+的平均消耗速率大于 0.15a mol/(L·h)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式______
(2)分子式为C6H12的某烃的所有碳原子都在同一平面上,则该烃的结构简式为_________,若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为__________。
(3)某芳香烃结构为![]() 。它的分子式为________,一氯代物有________种。
。它的分子式为________,一氯代物有________种。
(4)分子式为C8H10的芳香烃,苯环上的一氯代物只有一种,该芳香烃的结构简式是______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雷美替胺是首个没有列为特殊管制的非成瘾失眠症治疗药物,合成该有机物过程中涉及如下转化,下列说法不正确的是( )
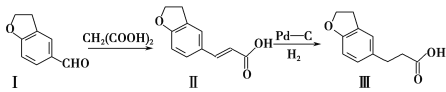
A.溴水无法区分化合物I和化合物Ⅱ
B.化合物Ⅰ、Ⅱ、Ⅲ均能与NaHCO3溶液发生反应
C.1 mol化合物Ⅲ最多能与3 mol H2发生加成反应
D.化合物Ⅰ、Ⅱ、Ⅲ分子中不存在手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用CO和H2生产燃料甲醇(CH3OH)。一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态)。下列说法错误的是

A.反应的化学方程式:CO+2H2CH3OH
B.反应进行至3分钟时,正、逆反应速率相等
C.反应至10分钟,(CO)=0.075mol/(L·min1)
D.反应至3分钟,用甲醇来表示反应的平均速率为![]() mol/(L·min1)
mol/(L·min1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其化合物在国民经济发展中起着重要作用。
(1)铜在潮湿的空气中能发生吸氧腐蚀而生锈,铜锈的主要成分为Cu2(OH)2CO3(碱式碳酸铜)。该过程中负极的电极反应式为_________。
(2)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其原理如图所示:

①根据下表数据,请你判断该电池工作的适宜温度应控制在_________。
物质 | Na | S | Al2O3 |
熔点/℃ | 97.8 | 115 | 2 050 |
沸点/℃ | 892 | 444.6 | 2 980 |
a.100 ℃以下 b.100 ℃~300 ℃
c.300 ℃~350 ℃ d.350 ℃~2 050 ℃
②放电时,电极A为_________极,S发生_________反应。
③放电时,内电路中Na+的移动方向为_________(填写“从A到B”或“从B到A”)。
④充电时,总反应为Na2Sx=2Na+Sx(3<x<5),Na所在电极与直流电源_________极相连,阳极的电极反应式________。
(3)某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。

①正极反应为_________。
②当电路中转移0.005 mol e-时,交换膜左侧溶液中约减少_________mol离子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质X的结构简式如图所示,它常用于制香料或作为饮料酸化剂,在医学上也有广泛用途。下列关于物质X的说法正确的是( )
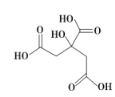
A.X的分子式为C6H7O7
B.X分子内所有原子均在同一平面内
C.1mol物质X最多可以和3mol氢气发生加成反应
D.足量的X分别与等物质的量的NaHCO3、Na2CO3反应得到的气体的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是( )
A.升温不利于正反应生成Ni(CO)4(g)
B.在25 ℃时,反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为2×10-5
C.在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol·L-1,则此时v正>v逆
D.在80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com