
���� ��1���������������ĵ��뷽��ʽ��дCr��OH��3�ĵ��뷽��ʽ��
��2��Cr2O72-+H2O?2CrO42-+2H+����H+Ũ������ʱ��ƽ�����淴Ӧ�ķ����ƶ�����OH-Ũ������ʱ����������H+����ʹƽ��������Ӧ�ķ����ƶ����ݴ˷�����
��� �⣺��1���������������ĵ��뷽��ʽ��дCr��OH��3�ĵ��뷽��ʽΪCrO2-+H++H2O?Cr��OH��3?Cr3++3OH-���ʴ�Ϊ��CrO2-+H++H2O?Cr��OH��3?Cr3++3OH-��
��2��Cr2O72-+H2O?2CrO42-+2H+����H+Ũ������ʱ��ƽ�����淴Ӧ�ķ����ƶ���������Cr2O72-�ķ����ƶ���������Һ�ʳȺ�ɫ����OH-Ũ������ʱ����������H+����ʹƽ��������Ӧ�ķ����ƶ��������� CrO42-�ķ����ƶ���������Һ�ʻ�ɫ���ʴ�Ϊ��Cr2O72-���Ⱥ죻CrO42-���ƣ�
���� ���⿼�黯ѧƽ���ƶ���Ӱ�죬ע��Cr2O72-+H2O?2CrO42-+2H+��ƽ���ƶ�����Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O2+C$\frac{\underline{\;����\;}}{\;}$CO2 | B�� | 2NaOH+CO2�TNa2CO3+H2O | ||
| C�� | 2Na2O2+CO2�T2Na2CO3+O2 | D�� | 2Mg+CO2$\frac{\underline{\;��ȼ\;}}{\;}$2MgO+C |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 AΪ���ʣ�B��C��D��EΪ��A������ͬԪ�صĻ��������֮��������ת����ϵ��
AΪ���ʣ�B��C��D��EΪ��A������ͬԪ�صĻ��������֮��������ת����ϵ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| λ�� | A��B��������� | ���Ӱ뾶�Ƚ� | ||||
| ���� | ���� | ���� | ||||
| Am+��Bn-����������Ӳ� | A | |||||
| B | ||||||
| Am+��Bn-���һ�����Ӳ� | A | |||||
| B | ||||||
| Am+��Bn-���Ӳ�ṹ��ͬ | A | |||||
| B | ||||||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

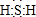 ����ˮ��Һ�����ڿ����з������ױ���ǣ��ñ仯���ֳ���S�ǽ����Ա�O��O���ǿ��������������ԭ�ӽṹ����ԭ��ͬ����Ԫ��������������ͬ�����ϵ��£����Ӳ������࣬ԭ�Ӱ뾶���õ�������������
����ˮ��Һ�����ڿ����з������ױ���ǣ��ñ仯���ֳ���S�ǽ����Ա�O��O���ǿ��������������ԭ�ӽṹ����ԭ��ͬ����Ԫ��������������ͬ�����ϵ��£����Ӳ������࣬ԭ�Ӱ뾶���õ��������������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��һ����100mlϡ���ᷴӦʣ4.8g����ΪCu��Fe | |
| B�� | ��Ӧǰϡ��������ʵ�����Ũ��Ϊ1.5 mol•L-1 | |
| C�� | �����������������Һ���ټ���������ϡ���ỹ�ɵõ������0.56LNO | |
| D�� | ԭ�������Cu��Fe�����ʵ����ֱ�Ϊ0.06mol��0.09mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
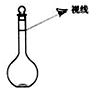
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.2��10-10 mol/L | B�� | 2.2��10-12 mol/L | C�� | 2.2��10-14 mol/L | D�� | 1.1��10-21 mol/L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com