
分析 铜与铁总质量为a g,与盐酸反应会生成氯化亚铁,滤液中加入过量氢氧化钠溶液反应后所得红棕色粉末为Fe2O3,Fe2O3的质量仍为a g,说明Cu的质量等于Fe2O3中O元素的质量.
解答 解:铜与铁总质量为a g,与盐酸反应会生成氯化亚铁,滤液中加入过量氢氧化钠溶液反应后所得红棕色粉末为Fe2O3,Fe2O3的质量仍为a g,说明Cu的质量等于Fe2O3中O元素的质量,则合金中Cu的质量分数等于Fe2O3中O元素的质量分数=$\frac{48}{160}$×100%=30%,
故答案为:30%.
点评 本题考查混合物有关计算,明确发生的反应找出合金中Cu与氧化物中氧元素质量关系是解答本题的关键,注意铁元素的守恒.


科目:高中化学 来源: 题型:选择题
| A. | 12.0 g熔融的NaHSO4中含有离子总数为0.2NA | |
| B. | 电解精炼Cu时,导线中通过2NAe-时,阳极质量减少64 g | |
| C. | 标准状况下,11.2 LCHCl3中含有的共用电子对数目为2NA | |
| D. | 标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烷的球棍模型为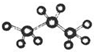 | B. | 丙烯的结构简式为CH3CHCH2 | ||
| C. | 符合通式CnH2n+2的一定是烷烃 | D. | O2、O3属于同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8% | B. | 9% | C. | 10% | D. | 5% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温下,浓硫酸不与铜反应,是因为铜被钝化 | |
| B. | 在BaC12溶液中通入SO2气体,溶液仍澄清,滴入3%过氧化氢溶液有白色沉淀 | |
| C. | 二氧化硫气体能用浓硫酸干燥,说明二氧化硫无还原性 | |
| D. | 硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷与氯气混合后光照发生反应 | B. | 乙炔与氯气的加成反应 | ||
| C. | 乙烯与氯化氢的加成反应 | D. | 二氧化碳通入石灰水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 500mL | B. | 600mL | C. | 650mL | D. | 700mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com