
将pH=13的NAOH平均分成两份,一份加适量的水,另一份加与该碱物质的量浓度相同的适量盐酸溶液后,pH都降低了1,则加入水与盐酸的体积比是( )
A.9 B.10 C.11 D.12
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
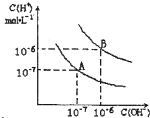 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
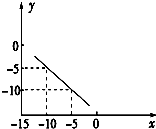 在某温度下的水溶液中,c(H+)=10x mol?L-1,c(OH-)=10ymol?L-1,x与y关系如图所示.
在某温度下的水溶液中,c(H+)=10x mol?L-1,c(OH-)=10ymol?L-1,x与y关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
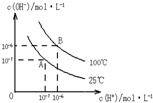 在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com