
【题目】25℃时,水的电离达到平衡:H2O![]() H++OH—ΔH>0,下列叙述正确的是( )
H++OH—ΔH>0,下列叙述正确的是( )
A.向水中加入氢氧化钠,平衡逆向移动,c(H+)降低,c(OH―)增大
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw变大
C.向水中加入少量固体CH3COOH,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,c(H+)不变
科目:高中化学 来源: 题型:
【题目】2018年10月3日瑞典皇家科学院宣布,将授予美国科学家弗朗西丝![]() 阿诺德、美国科学家乔治
阿诺德、美国科学家乔治![]() 史密斯和英国科学家格雷戈里
史密斯和英国科学家格雷戈里![]() 温特三位科学家2018年诺贝尔化学奖,以表彰他们在酶的定向演化以及用于多肽和抗体的噬菌体展示技术方面取得的成果。获奖者已经利用达尔文原理开发出造福人类的新型化学品。第一个药物阿达木单抗于2002年获批,用于治疗类风湿关节炎、银屑病和炎症性肠病,其结构式如图1所示:
温特三位科学家2018年诺贝尔化学奖,以表彰他们在酶的定向演化以及用于多肽和抗体的噬菌体展示技术方面取得的成果。获奖者已经利用达尔文原理开发出造福人类的新型化学品。第一个药物阿达木单抗于2002年获批,用于治疗类风湿关节炎、银屑病和炎症性肠病,其结构式如图1所示:
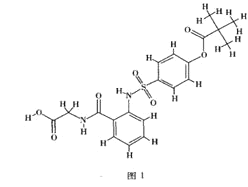
(1)阿达木单抗中碳原子的杂化方式为________,所含元素中前10号元素的电负性由小到大的顺序为________。
(2)弗朗西斯阿诺德主要研究酶的定向进化,金属酶含有一种或几种金属离子,金属酶种类很多,以含锌、铁、铜的酶最多,如铁金属酶一细胞色素,也有含有钼、锰等其他金属离子的酶。
![]() 基态Fe原子中,核外电子占据的轨道数为________,
基态Fe原子中,核外电子占据的轨道数为________,![]() 的价电子轨道表示式为________,检验
的价电子轨道表示式为________,检验![]() 常用KSCN溶液,其阴离子的等电子体为________
常用KSCN溶液,其阴离子的等电子体为________![]() 任写一种分子
任写一种分子![]() 。
。
![]() 与Fe属于同一周期,且核外最外层电子构型相同,但Ca的熔点沸点都比Fe低,原因是________。
与Fe属于同一周期,且核外最外层电子构型相同,但Ca的熔点沸点都比Fe低,原因是________。
(3)![]() 是人体多种酶的辅助因子,其与某有机物生成的配位离子
是人体多种酶的辅助因子,其与某有机物生成的配位离子![]() 图
图![]() 具有酶的某些特性。该离子中存在的化学键有________。
具有酶的某些特性。该离子中存在的化学键有________。
![]() 离子键
离子键 ![]() 共价键
共价键 ![]() 配位键
配位键 ![]() 氢键
氢键 ![]() 范德华力
范德华力

(4)如图3是晶体![]() 的结构,该晶体是一种磁性材料,能导电。
的结构,该晶体是一种磁性材料,能导电。
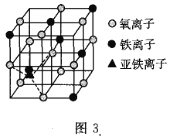
![]() 晶胞中铁离子处于氧离子围成的________
晶胞中铁离子处于氧离子围成的________![]() 填空间结构
填空间结构![]() 空隙。
空隙。
![]() 若晶胞的体对角线长为
若晶胞的体对角线长为![]() ,则
,则![]() 晶体的密度为________
晶体的密度为________![]()
![]() 阿伏加德罗常数用
阿伏加德罗常数用![]() 表示
表示![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素铬![]() 在溶液中主要以
在溶液中主要以![]() 蓝紫色
蓝紫色![]() 、
、![]() 绿色
绿色![]() 、
、![]() 橙红色
橙红色![]() 、
、![]() 黄色
黄色![]() 等形式存在,
等形式存在,![]() 为难溶于水的灰蓝色固体,回答下列问题:
为难溶于水的灰蓝色固体,回答下列问题:
(1)![]() 与
与![]() 的化学性质相似,在
的化学性质相似,在![]() 溶液中逐滴加入NaOH溶液直至过量,可察到的现象是 ______________________________________________ .
溶液中逐滴加入NaOH溶液直至过量,可察到的现象是 ______________________________________________ .
(2)![]() 和
和![]() 在溶液中可相互转化
在溶液中可相互转化![]() 室温下,初始浓度为
室温下,初始浓度为![]() 的
的![]() 溶液中
溶液中![]() 随
随![]() 的变化如图所示.
的变化如图所示.
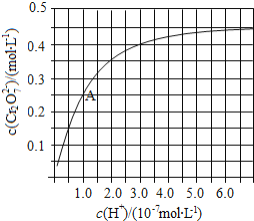
![]() 用离子方程式表示
用离子方程式表示![]() 溶液中的转化反应______________________________ .
溶液中的转化反应______________________________ .
![]() 由图可知,溶液酸性增大,
由图可知,溶液酸性增大,![]() 的平衡转化率__________________
的平衡转化率__________________ ![]() 填“增大“减 小”或“不变”
填“增大“减 小”或“不变”![]() 根据A点数据,计算出该转化反应的平衡常数为 _______________ .
根据A点数据,计算出该转化反应的平衡常数为 _______________ .
![]() 升高温度,溶液中
升高温度,溶液中![]() 的平衡转化率减小,则该反应的
的平衡转化率减小,则该反应的![]() ______
______ ![]() 填“大于”“小于”或“等于”
填“大于”“小于”或“等于”![]() .
.
(3)在化学分析中采用![]() 为指示剂,以
为指示剂,以![]() 标准溶液滴定溶液中的
标准溶液滴定溶液中的![]() ,利用
,利用![]() 与
与![]() 生成砖红色沉淀,指示到达滴定终点
生成砖红色沉淀,指示到达滴定终点![]() 当溶液中
当溶液中![]() 恰好完全沉淀
恰好完全沉淀![]() 浓度等于
浓度等于![]() 时,溶液中
时,溶液中![]() 为 ______
为 ______ ![]() ,此时溶液中
,此时溶液中![]() 等于 ______
等于 ______ ![]() 已知
已知![]() 、AgCl的
、AgCl的![]() 分别为
分别为![]() 和
和![]()
(4)![]() 价铬的化合物毒性较大,常用
价铬的化合物毒性较大,常用![]() 将废液中的
将废液中的![]() 还原成
还原成![]() ,反应的离子方程式为 _________________________________________________ .
,反应的离子方程式为 _________________________________________________ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列叙述的方法中,能将有机化合物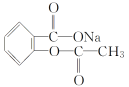 转变为
转变为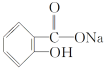 的有( )
的有( )
①跟足量NaOH溶液共热后,通入二氧化碳直至过量
②与稀硫酸共热后,加入足量Na2CO3溶液
③与稀硫酸共热后,加入足量NaOH溶液
④与稀硫酸共热后,加入足量NaHCO3溶液
⑤与足量的NaOH溶液共热后,再加入适量H2SO4
A.①②B.②③
C.③④D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃分子的球棍模型(如图),据此回答下列问题:

(1)等质量的上述烃燃烧耗氧量最高的是(填对应字母)__;
(2)属于同系物的是(填对应字母)___;
(3)所有原子都在同一平面上的是(填对应字母)___;
(4)一卤代物总类最多的是(填对应字母)___;
(5)实验室制D的化学方程式___;
(6)写出G合成烈性炸药(TNT)的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含有PbI2固体的饱和溶液中存在着平衡PbI2(s)![]() Pb2+(aq)+2I(aq),加入KI固体,下列说法正确的是( )
Pb2+(aq)+2I(aq),加入KI固体,下列说法正确的是( )
A.溶液中Pb2+和I的浓度都增大B.溶度积常数Ksp增大
C.沉淀溶解平衡向右移动D.溶液中Pb2+的浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H3PO4是三元酸,如图是在常温下溶液中含磷微粒的物质的量分数(δ)随pH变化示意图。下列说法不正确的是( )
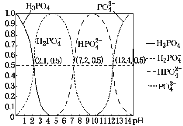
A.磷酸的第二级电离平衡常数约为10-7.2
B.在NaH2PO4溶液中:c(HPO42-)>c(H3PO4-)
C.在磷酸中滴加NaOH溶液至pH=7,c(Na+)=2c(HPO42)+c(H2PO4)
D.Na3PO4溶液中:c(Na+)=3c(PO43-)+3c(HPO42-)+3c(H2PO4-)+3c(H3PO4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A.乙醇和丙三醇互为同系物
B.环己烯(![]() )分子中的所有碳原子共面
)分子中的所有碳原子共面
C.分子式为C5H10O2,且属于酯的同分异构体共有9种(不考虑立体异构)
D.桥环烃二环[2,2,0](![]() )的二氯代物有6种结构(不考虑立体异构)
)的二氯代物有6种结构(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应对应的反应类型正确的是
A.2CH3CHO+O2![]() 2CH3COOH 氧化反应
2CH3COOH 氧化反应
B.2CH3OH![]() CH3OCH3+H2O 消去反应
CH3OCH3+H2O 消去反应
C.nHOCH2CH2OH![]() 加聚反应
加聚反应
D.CH2=CH2 + Cl2![]() CH2=CHCl + HCl 加成反应
CH2=CHCl + HCl 加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com