
近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应的化学方程式为:KI+3H2O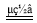 KIO3+3H2↑。下列有关说法不正确的是 ( )
KIO3+3H2↑。下列有关说法不正确的是 ( )
A.电解转移3 mol e-时,理论上可制得KIO3 107 g
B.电解时, 石墨作阳极,不锈钢作阴极
C.电解时的阳极电极反应式:I-?6e-+3H2O = IO3-+6H+
D.电解过程中电解质溶液的pH变小
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案科目:高中化学 来源:2015届湖北省咸宁市高三三校联考化学试卷(解析版) 题型:填空题
(8分)氧化还原反应实际上包含氧化反应和还原反应两个过程,一个还原反应过程的离子方程式为:NO+4H++3e-===NO↑+2H2O。下列四种物质:KMnO4、Na2CO3、KI、Fe2(SO4)3中的一种物质甲,滴加少量稀硝酸,能使上述反应过程发生。
(1)被还原的元素是________;还原剂是________。
(2)写出并配平该氧化还原反应方程式:________________________________________。
(3)反应生成0.3 mol H2O,则转移电子的数目为____________。
(4)若反应后,氧化产物的化合价升高,而其他物质保持不变,则反应中氧化剂与还原剂的物质的量之比将________(填“增大”、“不变”、“减小”或“不能确定”)。
查看答案和解析>>
科目:高中化学 来源:2015届海南省高三第四次月考化学试卷(解析版) 题型:选择题
在标准状况下,如果2.8L氧气含有n个氧原子,则阿伏加德罗常数可表示为
A.n/8mol-1 B.n/16 mol-1 C.8n mol-1 D.4n mol-1
查看答案和解析>>
科目:高中化学 来源:2015届浙江省协作体高三第一次适应性测试理科综合化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.向Na2CO3溶液通入CO2,可使水解平衡:CO32 -+H2O HCO3- +OH-向正反应方向移动,则溶液pH增大
HCO3- +OH-向正反应方向移动,则溶液pH增大
B.室温时,0.1 mol·L-1某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4
C.25 ℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA
D.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH值
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期回头考试化学试卷(解析版) 题型:选择题
氯碱工业的产物NaOH与不同物质反应可以生成不同的盐。已知常温下,浓度均为0.1 mol/L的4种钠盐溶液pH如下表:
溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
pH | 11.6 | 9.7 | 10.3 | 5.2 |
下列说法中, 正确的是( )
A.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是H2SO3
D.NaHSO3溶液中离子浓度大小顺序为c(Na+)> c(H+)>c(HSO3-) >c(SO32-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期回头考试化学试卷(解析版) 题型:选择题
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl = Na2Mn5O10+2AgCl 下列“水” 电池在海水中放电时的有关说法正确的是( )
A.正极反应式:Ag+Cl--e-== AgCl
B.每生成1 mol Na2Mn5O10转移2 mol电子
C.Na+不断向“水”电池的负极移动
D.AgCl是还原产物
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期回头考试化学试卷(解析版) 题型:选择题
下列各组物质的性质比较,正确的是( )
A.熔点:CO2<H2O<SiO2<KCl B.粒子半径:K+>Na+>Mg2+>Al3+
C.酸性:H3PO4>H2SO4>HClO4>H2SiO3 D.稳定性:H2O<NH3<PH3<SiH4
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三第一次联考化学试卷(解析版) 题型:选择题
下列表格中的各种情况,可以用下面的图象曲线表示的是
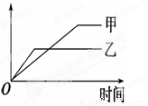
| 反应 | 纵坐标 | 甲 | 乙 |
A | 等质量的钾、钠分别与足量水反应 | H2质量 | 钠 | 钾 |
B | 相同质量氨,在同一容器中2NH3 | 氨气的转化率 | 500℃ | 400℃ |
C | 在体积可变的恒压容器中,体积比1:3的N2、H2,2NH3 | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
D | 2molSO2与1molO2,在相同温度下2SO2+O2 | SO3物质的量 | 10个大气压 | 2个大气压 |
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三9月月考化学试卷(解析版) 题型:选择题
已知单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点就越高.则下列溶液沸点最高的是( )
A.0.01 mol/L的蔗糖溶液 B.0.01 mol/L的CaCl2溶液
C.0.02 mol/L的NaCl溶液 D.0.02 mol/L的CH3COOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com