
����Ŀ��A��B��C��D��EΪԭ��������������Ķ�����Ԫ�أ���֪A��B��E3��ԭ������㹲��11�����ӣ�����3��Ԫ�ص�����������ˮ�����������ܷ�����Ӧ�����κ�ˮ��CԪ�ص������������ȴ�����������4��DԪ��ԭ�Ӵ�����������������������3��
��1��д��Ԫ�ص����ƣ�C �� D��
��2��д��Ԫ�ص�ԭ�ӽṹͼ��
A �� B �� �������Ӱ뾶���������ӷ��ţ���
��3��A��B������������ˮ����ļ��������ѧʽ����ͬ��
��4��D��E����̬�⻯����ȶ��ԣ��� ��
���𰸡�
��1��Si��P
��2��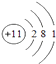 ��
��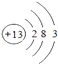 ��Na+��Al3+
��Na+��Al3+
��3��NaOH��Al��OH��3
��4��HCl��PH3
���������⣺A��B��C��D��EΪԭ��������������Ķ�����Ԫ�أ�CԪ�ص������������ȴ�����������4����CԪ��ԭ����3�����Ӳ㣬����������Ϊ4����CΪSiԪ�أ�DԪ��ԭ���������ڹ�Ԫ�أ����ڵ������ڣ�DԪ��ԭ�Ӵ�����������������������3��������������Ϊ8��3=5����DΪ��Ԫ�أ�A��B��E����Ԫ�ص�����������ˮ�����������ܷ�����Ӧ�����κ�ˮ��Ӧ������������ǿ�ᡢǿ��֮��ķ�Ӧ����AΪNa��BΪAl������ԭ������㹲��11�����ӣ���E������������Ϊ11��1��3=7����EΪClԪ�أ���1�������Ϸ�����֪��CΪSi��DΪP�����Դ��ǣ�Si��P����2��AΪNa��ԭ�ӽṹʾ��ͼΪ 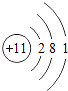 ��BΪAl��ԭ�ӽṹʾ��ͼΪ��
��BΪAl��ԭ�ӽṹʾ��ͼΪ�� 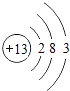 ��Na+��Al3+���ӶԳƽṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶��Na+��Al3+ ��
��Na+��Al3+���ӶԳƽṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶��Na+��Al3+ ��
���Դ��ǣ� 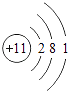 ��
�� 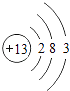 ��Na+��Al3+����3��������Խǿ������������ˮ����ļ���Խǿ��������Na��Al������ԣ�NaOH��Al��OH��3 �� ���Դ��ǣ�NaOH��Al��OH��3����4��ͬ����������ҷǽ�������ǿ��Ԫ�صķǽ�����Խǿ���⻯��Խ�ȶ������⻯���ȶ��ԣ�HCl��PH3 �� ���Դ��ǣ�HCl��PH3 ��
��Na+��Al3+����3��������Խǿ������������ˮ����ļ���Խǿ��������Na��Al������ԣ�NaOH��Al��OH��3 �� ���Դ��ǣ�NaOH��Al��OH��3����4��ͬ����������ҷǽ�������ǿ��Ԫ�صķǽ�����Խǿ���⻯��Խ�ȶ������⻯���ȶ��ԣ�HCl��PH3 �� ���Դ��ǣ�HCl��PH3 ��


 ��ĩ100�ִ��غ�������ϵ�д�
��ĩ100�ִ��غ�������ϵ�д� Сѧ�������Ծ�ϵ�д�
Сѧ�������Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ϊ�ж�����������Ԫ�طǽ�����ǿ����������
A. ���ʵ������� B. ���ʵ��ȶ���
C. ��̬�⻯��ķе� D. �����ӵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У��ı䷴Ӧ���������Ũ�ȣ�����ı����������
A. ͭ�����ᷴӦ B. ������̼ͨ������������Һ��
C. ��������ķ�Ӧ D. �Ȼ����백ˮ�ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(1100���������ܱ������з�����Ӧ��Na2SO4(s��+4H2(g��![]() Na2S(s��+4H2O(g��������˵����ȷ����( ��
Na2S(s��+4H2O(g��������˵����ȷ����( ��
A���÷�Ӧ��ƽ�ⳣ������ʽK=c(H2O��/c(H2��
B����������������ܶȻ�ѹǿ���ֲ��䣬��˵���÷�Ӧ�Ѵﵽƽ��״̬
C����Na2SO4�������ı���ʼ����H2��Ũ�ȣ���ƽ��ʱH2��ת���ʲ���
D������ʼʱͶ��2.84gNa2SO4��һ����H2����Ӧ��ƽ��ʱ�����ڹ��干��2.264g����Na2SO4��ת����Ϊ50%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ԭCO2�ǽ������ЧӦ����Դ�������Ҫ�ֶ�֮һ���о���������Cu/ZnO���������£�CO2��H2�ɷ�������ƽ�з�Ӧ���ֱ�����CH3OH��CO����Ӧ���Ȼ�ѧ����ʽ���£�
CO2��g��+3H2��g��![]() CH3OH��g��+H2O��g����H1=-53.7kJ��mol-1 I
CH3OH��g��+H2O��g����H1=-53.7kJ��mol-1 I
CO2��g��+H2��g��![]() CO��g��+H2O��g����H2 II
CO��g��+H2O��g����H2 II
ijʵ���ҿ���CO2��H2��ʼͶ�ϱ�Ϊ1:2.2������ͬѹǿ�£�������ͬ��Ӧʱ��������ʵ�����ݣ�
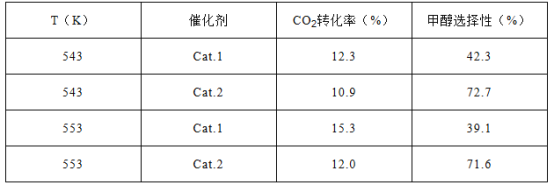
����ע������.1:Cu/ZnO���װ�������.2:Cu/ZnO����Ƭ���״�ѡ���ԣ�ת����CO2�����ɼ״��İٷֱ�
��֪����CO��H2�ı�ȼ���ȷֱ�Ϊ-283.0kJ��mol-1��-285.8kJ��mol-1
��H2O��l��![]() H2O��g����H3=44.0kJ��mol-1
H2O��g����H3=44.0kJ��mol-1
��ش𣨲������¶ȶ���H��Ӱ�죩��
��1����ӦI��ƽ�ⳣ������ʽK=_________����ӦII����H2=_____________kJ��mol-1��
��2�����������CO2ת��ΪCH3OHƽ��ת���ʵĴ�ʩ��_________________��
A��ʹ�ô���.1 B��ʹ�ô���.2 C�����ͷ�Ӧ�¶�
D��Ͷ�ϱȲ��䣬���ӷ�Ӧ���Ũ�� E������CO2��H2�ij�ʼͶ�ϱ�
��3������ʵ�����ݱ���������ͬ�¶��²�ͬ�Ĵ�����CO2ת����CH3OH��ѡ������������Ӱ�죬��ԭ����__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ�Ե���ʡ��ǵ���ʵĶ����жϣ�����������ȷ����
A. ��Ȼʯī�нϺõĵ����ԣ��������ڷǵ����
B. ʵ����NH3��CO2��ˮ��Һ���ܵ��磬����NH3��CO2���ǵ����
C. ʵ����Һ̬HCl������NaCl�����ܵ��磬����HCl��NaCl���Ƿǵ����
D. ���ǣ��������ˮ��Һ������״̬�¾����ܵ��磬�����������ڷǵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��t��ʱ����2molSO2��1molO2ͨ�����Ϊ2L�ĺ��º����ܱ������У��������·�Ӧ��
2SO2��g��+ O2��g��![]() 2SO3��g������H=��196.6 kJ/mol��2 minʱ��Ӧ�ﵽ��ѧƽ�⣬��ʱ��÷�Ӧ��O2������0.8 mol������д���пհף�
2SO3��g������H=��196.6 kJ/mol��2 minʱ��Ӧ�ﵽ��ѧƽ�⣬��ʱ��÷�Ӧ��O2������0.8 mol������д���пհף�
��1���ӷ�Ӧ��ʼ���ﻯѧƽ�⣬����SO3��ƽ����Ӧ����Ϊ ��ƽ��ʱSO2ת����Ϊ ��
��2������������֤���÷�Ӧ�Ѵﵽ��ѧƽ��״̬���ǣ����ţ���ͬ�� ��
A��������ѹǿ���ٷ����仯
B��SO2������������ٷ����仯
C������������ԭ���������ٷ����仯
D����ͬʱ��������2nmolSO2��ͬʱ����nmolO2
E����ͬʱ��������2nmolSO2��ͬʱ����nmolO2
��3����Ӧ�ﵽ��ѧƽ������²���������ƽ�������������ƶ��������SO2ת���ʵ��� ��
A����������ͨ������O2 B����������ͨ������SO2
C��ʹ�ô��� D�������¶�
E����������ͨ��������������֪��������SO2��O2��SO3����������Ӧ��
��4��t2��ʱ���������ʵ���֮��n(SO2����n(O2)=1��1�Ļ������ͨ��һ�����º�ѹ���ܱ������У���Ӧ�ﵽƽ��ʱ������������������20%��SO2��ת����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���������
A. �κλ�ѧ��Ӧ�������������仯
B. ��ѧ��Ӧ�������仯�Ĵ�С�뷴Ӧ�������������
C. ��ѧ�仯�е������仯��Ҫ���ɻ�ѧ���仯�����
D. �����仯�ǻ�ѧ��Ӧ�Ļ�������֮һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У�������Ȼ�߷��ӻ��������
A. ���� B. ��֬ C. ������ D. ����ϩ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com