
ij��ѧС��ͬѧ��һ���������������۵�NaHSO3��Һ�м����Թ�����KIO3��Һ��һ��ʱ�����ҺͻȻ����ɫ��
��1����������֪NaHSO3�����KIO3��Ӧ��Ϊ�����������У���һ��ΪIO3��+ 3HSO3��=3SO42��+3H+ + I������ڶ�����Ӧ�����ӷ���ʽΪ_____________________________
��2��ͨ���ⶨ��Һ��������ʱ��̽��Ũ�Ⱥ��¶ȶԸ÷�Ӧ�ķ�Ӧ���ʵ�Ӱ�졣���ڷ�Ӧ��Ũ�Ⱥ��¶Ƚ��жԱ�ʵ�飬��¼���£�
| ʵ���� | 0.02mol/LNaHSO3��Һ/mL | 0.02mol/LKIO3��Һ/mL | H2O/mL | ��Ӧ�¶�/�� | ��Һ������ʱ��t/s |
| �� | 15 | 20 | 10 | 15 | t1 |
| �� | a | 30 | 0 | 15 | t2 |
| �� | 15 | b | c | 30 | t3 |
ʵ��٢���̽��______________�Է�Ӧ���ʵ�Ӱ�죬����a=________��ʵ��٢���̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죬�����b=________��c=________
��3����NaHSO3��Һ��KIO3��Һ���(Ԥ�ȼ�������Ե���Ϊָʾ��)�������ʼ���Ǽ�����ʼ�η�Ӧ����������һ��ʱ���Ӧ��������С�����������ʼ�η�Ӧ�����������ԭ��������¼��裬������ɼ�������
����һ����Ӧ���ɵ�SO42���Է�Ӧ������ã�SO42��Ũ��Խ��Ӧ����Խ�죻
���������Ӧ���ɵ�H+�Է�Ӧ������ã�H+Ũ��Խ��Ӧ����Խ�죻
��������__________________________________________________________��
����
��4���������ʵ����֤��������һ������±������ݣ���Ӧ���ʿ��ò����Dzⶨ��
| ʵ�鲽�裨��Ҫ��д������������̣� | Ԥ��ʵ������ͽ��� |
��13�֣�
��1��IO3�� + 5I�� + 6H+ = 3I2 + 3H2O��2�֣�
��2��KIO3��Һ ��Ũ�ȣ�15��20��10����1�֣�
��Ũ�ȣ�15��20��10����1�֣�
��3������������Ӧ���ɵ�I���Է�Ӧ������ã�I��Ũ��Խ��Ӧ����Խ�죨2�֣�
(��Ӧ���ɵ�I2�Է�Ӧ������ã�I2Ũ��Խ��Ӧ����Խ�죻��÷�Ӧ�Ƿ��ȷ�Ӧ���¶����ߵ��·�Ӧ���ʼӿ죨2�֡���С����п����ԣ��𰸺��������֣�
��4��
| ʵ�鲽�裨��Ҫ��д������������̣� | Ԥ��ʵ������ͽ��� |
| ���ձ����н�NaHSO3��Һ�����KIO3��Һ��ϣ��ò����Dzⶨ����ʼʱ�ķ�Ӧ����v(��)�����ձ����н���ͬһ��Ӧ����ͬ�������ձ���Ԥ�ȼ�������Na2SO4��K2SO4��ĩ��������Ӧ��������ȫ��ͬ�����ⶨ����ʼ�ε���ͬʱ���ڵķ�Ӧ����v(��)��3�֣� | ��v(��) = v(��)�������һ�������� ��v(��)��v(��)�������һ��������2�֣� |


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�±����������У�����֮��������ʵ����ͼ��ʾת������
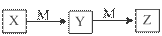
| ѡ�� | X | Y | Z | M |
| A | NH3 | NO | NO2 | O2 |
| B | Cl2 | FeCl3 | FeCl2 | Fe |
| C | Al | Al(OH)3 | NaAlO2 | NaOH |
| D | NaOH | Na2CO3 | NaHCO3 | CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ӹ�������A�������Է������¿�ͼ��ʾ��һϵ�б仯��
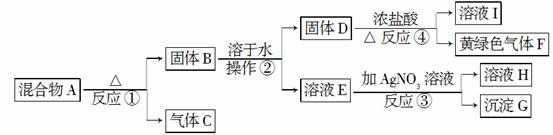
GΪ������ϡ����İ�ɫ���壻��ҺH����ɫ��Ӧ����ɫ(����ɫ���ܲ����۲�)���ش��������⣺
(1)��ʵ�������ռ�����C����ѡ����ͼװ���е�________��

(2)�����ڵ�������________���ڲ���������ʹ�õIJ���������������________���ڵõ�����Dʱ�������ϴ�ӡ�����Ȳ�����ϴ�ӹ���D��Ŀ����________________________________________��
(3)д����Ӧ�ٵĻ�ѧ����ʽ����Ӧ�ܵ����ӷ���ʽ��
��Ӧ�٣�_____________________________________________��
��Ӧ�ܣ�___________________________________________��
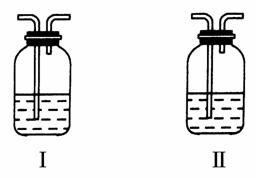
(4)��ʵ�����У�Ҫ��ø��﴿���Ļ���ɫ����F�����Խ�������ͨ����ͼ�еĢ�װ�ã�����ƿ����ʢ�ŵ���________��ƿ����ʢ�ŵ���________��
(5)ʵ���б������ն��������F��������Ⱦ��������ͼ��ʵ������NaOH��Һ��������F��װ�ã�Ϊ��ֹ����������������װ����________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1����֪��������ͨ����������S8(б����)����ʽ���ڣ���������״̬ʱ������S2��S4��S6��
S8�ȶ���ͬ�������壬����S4��S6��S8�������ƵĽṹ�ص㣬��ṹ����ͼ��ʾ��

����һ���¶��£������������ƽ��Ħ������Ϊ80 g·mol��1�����������S2���ӵ����������С��__________��
������֪�������ļ���Ϊd kJ·mol��1���������ļ���Ϊe kJ·mol��1��S(s)��O2(g)===SO2(g)����H����a kJ·mol��1����S8����������ļ���Ϊ____________��
��2���±��Dz��ֻ�ѧ���ļ������ݣ�
| ��ѧ�� | P—P | P—O | O===O | P===O |
| ����(kJ·mol��1) | 198 | 360 | 498 | X |
����֪����ȼ����Ϊ2 982 kJ·mol��1������(P4)��P4O6��P4O10�ṹ����ͼ��ʾ��
���ϱ���X��________��

��0.5 mol����(P4)��O2��ȫ��Ӧ���ɹ�̬P4O6���ų�������Ϊ________kJ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���¶��£�������X������Y��0.16 mol����10 L�����ܱ������У�������Ӧ��X(g)+Y(g) ⇌ 2Z(g) ��H<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���

����˵������ȷ���� ( )
A�����¶��´˷�Ӧ��ƽ�ⳣ��K=1.44
B�������������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰ (��)<
(��)<  (��)
(��)
C����Ӧǰ2 min��ƽ������v (Z)=4. 0��10-3mol��(L��min)
0��10-3mol��(L��min)
D�������������䣬�ٳ���0.2 mol Z��ƽ��ʱX�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NAΪ�����ӵ�����������˵����ȷ����(����)
A��32 g O2���庬�е���ԭ����ΪNA
B��2 L 0.3 mol/L Na2SO4��Һ�к���Na��Ϊ0.6NA
C��27 g����ȫ��Ӧ��ʧȥ�ĵ�����Ϊ3NA
D��11.2 L���������ķ�����Ϊ0.5NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ���������������ӷ���ʽ����ȷ����(����)
A������þ��ϡ���ᷴӦ���������ݳ���Mg��2H����2Cl��===MgCl2��H2��
B���Ȼ�����Һ��ϡ���ᷴӦ���а�ɫ�������ɣ�Ba2����SO ===BaSO4��
===BaSO4��
C��̼���������ᷴӦ���������ݳ���Na2CO3��2H��===CO2����H2O��2Na��
D������ͭ��Һ�м��������NaOH��Һ���а�ɫ����������Cu2����2OH��===Cu(OH)2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ڷ�ӦA(g)+3B(g)  2C(g)�����и����ݱ�ʾ��ͬ�����µķ�Ӧ���ʣ����з�Ӧ���е������ǣ� ��
2C(g)�����и����ݱ�ʾ��ͬ�����µķ�Ӧ���ʣ����з�Ӧ���е������ǣ� ��
A��v(A)=0.01 mol/(L•s) B��v(B)=0.02 mol/(L•s)
C��v(B)=0.60mol/(L•min) D��v(C)=1.0mol/(L•min)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�á���ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش�
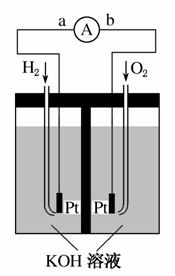
(1)����ȼ�ϵ�ص�����ת����Ҫ��ʽ��________________���ڵ����е�����������Ϊ________(��a��b��ʾ)��
(2)������ӦʽΪ___________________________________��
(3)�缫����Ʋ��۵�ԭ��Ϊ_________________________��
(4)�õ�ع���ʱ��H2��O2�������ⲿ��������ؿ����������ṩ���ܡ���ˣ�������ȫ�����ǹؼ�����֮һ���������һ����Ҫ�Ĵ�����ϣ�����ͷ���ԭ�����£�
��.2Li��H2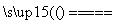 2LiH
2LiH
��.LiH��H2O===LiOH��H2��
�ٷ�Ӧ���еĻ�ԭ����________����Ӧ���е���������________��
����֪LiH�����ܶ�Ϊ0.82 g/cm3���������224 L(��״��)H2�����ɵ�LiH����뱻���յ�H2�����Ϊ________��
���ɢ����ɵ�LiH��H2O���ã��ų���H2�������ȼ�ϣ�������ת����Ϊ80%��������ͨ�����ӵ����ʵ���Ϊ________mol��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com