
| A、它的核外电子排布式为1s22s22p63s23p4 |
| B、它的元素符号为O |
| C、它可与H2生成液态化合物 |
D、轨道表示式为: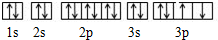 |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、把pH=6的盐酸稀释1000倍 |
| B、把pH=8的NaOH溶液稀释10倍 |
| C、把10mL 1×10-5mol/L的H2SO4溶液与10mL 4×10-5mol/L的NaOH溶液相混合 |
| D、把c(OH-)=10-5mol/L的NaOH溶液10mL加到100mL浓度为10-4mol/L的NaOH溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金刚石硬度大于硅,其熔点也高于硅 |
| B、HF、HCl、HBr、HI热稳定性依次减弱 |
| C、NaF、NaCl、NaBr、NaI的熔点依次降低 |
| D、F2、Cl2、Br2、I2的熔、沸点逐渐升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2ω1=ω2 |
| B、2ω2=ω1 |
| C、ω2>2ω1 |
| D、2ω1>ω2>ω1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、白水桶的成分是铁锌合金 |
| B、生铁含碳量比普通钢要高,所以硬而脆 |
| C、不锈钢是铁与铬镍的合金,不易生锈,但成本较贵 |
| D、铁元素是人体的常量元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO4=2H++SO42- |
| B、Al2(SO4)3=2Al3++3 SO42- |
| C、NaHCO3=Na++H++CO32- |
| D、Ba(OH)2=Ba2++2 OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com