
下列说法正确的是
A.钠是一种强还原剂,可以将钛、铌等金属从其氯化物溶液中置换出来
B.铜能与氯化铁溶液反应,该反应可以应用于印刷电路板的制作
C.人们发现了118种元素,即共有118种核素
D.H2和D2互为同位素
科目:高中化学 来源:2017届黑龙江牡丹江第一高级中学高三12月月考化学卷(解析版) 题型:选择题
在2L密闭容器中进行反应C(s)+H2O(g) CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
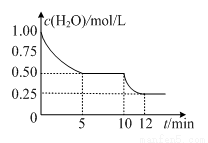
A.5min时该反应的K值一定小于12 min时的K值
B.0~5min内,v (H2)=0.05mol/(L•min)
C.10 min时,改变的外界条件可能是减小压强
D.该反应混合气体的平均相对分子质量:5min时小于12 min 时的
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江哈尔滨三中高三上验收考试三化学卷(解析版) 题型:选择题
下列叙述正确的是
A.化学键存在于原子之间,也存在于分子之间
B.离子键是阴、阳离子之间的吸引力
C.离子化合物可以含共价键
D.分子间作用力越大,分子越稳定
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学试卷(解析版) 题型:选择题
下列实验操作或叙述中正确的是
A. 蒸发操作时,应使混合物中的水分完全蒸干后再停止加热
B. 蒸馏时,温度计水银球需靠近蒸馏烧瓶支管口,冷凝水的流向需从冷凝管的上口进下口流出
C. 过滤后洗涤沉淀时,应将固体转移至烧杯中,并加入适量蒸馏水充分搅拌后再过滤
D. 分液时,先从分液漏斗下口放出下层液体,更换烧杯后再从上口放出上层液体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学试卷(解析版) 题型:选择题
对于中学某些常见离子的检验及结论—定正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32-
B.加入氯化钡溶液有白色沉淀产生,再加盐酸沉淀不消失,一定有SO42-
C.加入氯化钠溶液有白色沉淀产生,再加稀硝酸沉淀不消失,一定有Ag+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,—定有Ba2+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:填空题
⑴室温时,pH=a的氨水与PH =b的盐酸等体积混合,恰好完全反应,则氨水电离度可表示为_______________ (用百分数来表示)
(2)室温下,0.1 mol/LNaClO溶液的pH_________0.1 mol/LNa2SO3溶液的pH。(选填“大于”、“小于”,或“等于”)。浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为 。
已知:
H2SO3 | Kal=1.54×l0-2 | Ka2=1.02×10-7 |
HCIO | Ka1=2.95×10-8 | |
H2CO3 | Kal=4.3×10-7 | Ka2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
在溶液中能共存,加OH-有沉淀析出,加H+能放出气体的是
A.Na+、Cu2+、Cl-、SO42-
B.AlO2-、K+、CO32-、 Na+
C.Cl-、Al3+、 NH4+、HCO3-
D.Na+、Ca2+ 、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
mX(g)+nY(g)  qZ(g) △H<0, m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
qZ(g) △H<0, m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
A.通入稀有气体使压强增大,平衡将正向移动
B.X的正反应速率是Y的逆反应速率的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.若平衡时X、Y的转化率相等,说明反应开始时X、Y的物质的量之比为n:m
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上月考三化学试卷(解析版) 题型:实验题
I.硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀 锡工业。某研究小组设计SnSO4制备路线如下:
锡工业。某研究小组设计SnSO4制备路线如下:
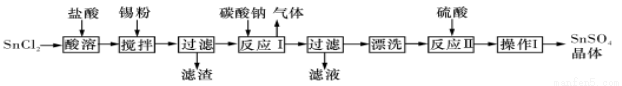
查阅资料:
A.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
B.SnC12易水解生成碱式氯化亚锡
回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,请结合必要的化学方程式用平衡移动原理解释原因:___________。
(2)加入Sn粉的作用有两个:①调节溶液pH;②__________。
(3)反应I得到沉淀SnO,得到该沉淀的离子反应方程式是____________。
(4)操作I是____________。
II.已知25℃时,AgI饱和溶液中c(Ag+)为1.22×10-8 mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10-5 mol/L。若在10 mL含有KCl和KI各为0.01 mol/L的溶液中,加入16 mL 0.01 mol/L AgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是
c(K+)>c(NO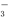 )>c(Cl-)>c(Ag+)>c(I-)
)>c(Cl-)>c(Ag+)>c(I-)
B .c(K+)>c(NO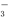 )>c(Ag+)>c(Cl-)>c(I-)
)>c(Ag+)>c(Cl-)>c(I-)
C.c(K+)>c(NO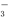 )>c(Ag+)=c(Cl-)+c(I-)
)>c(Ag+)=c(Cl-)+c(I-)
D.c(NO )>c(K+)>c(Ag+)>c(Cl-)>c(I-)
)>c(K+)>c(Ag+)>c(Cl-)>c(I-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com