
分析 (1)相同条件下,密度之比等于相对分子质量之比,据此计算混合气体的相对分子质量,进而确定含有的烷烃;
(2)剩余气体为烷烃,根据n=$\frac{V}{{V}_{m}}$计算44.8L混合气体及烷烃的物质的量,进而计算烯烃的物质的量;
(3)溴水质量增重28g为烯烃的质量,根据M=$\frac{m}{n}$计算其摩尔质量,结合烯烃的组成通式计算烯烃的分子式,进而书写可能的结构.
解答 解:(1)在同温同压下,混合气体对氢气的相对密度为13,故混合气体的平均相对分子质量为13×2=26,故一定含有甲烷,
故答案为:CH4;
(2)标况下44.8L混合气体的物质的量为$\frac{44.8L}{22.4L/mol}$=2mol,剩余气体为烷烃,故甲烷的物质的量为$\frac{33.6L}{22.4L/mol}$=$\frac{24g}{16g/mol}$=1.5mol烯烃的物质的量为2mol-1.5mol=0.5mol,故n(CH4):n(烯烃)=1.5mol:0.5mol=3:1,
故答案为:3:1;
(3)溴水质量增重28g为烯烃的质量,烯烃的摩尔质量为$\frac{28g}{0.5gmol}$=56g/mol,令烯烃的组成为(CH2)n,故14n=56,解得n=4,故该烯烃为C4H8,可能的结构为:CH2=CH-CH2CH3,CH3-CH=CH-CH3,CH2=C(CH3)2,
故答案为:CH2=CH-CH2CH3,CH3-CH=CH-CH3,CH2=C(CH3)2.
点评 本题考查有机物的分子式的确定、混合物计算、同分异构体等,难度中等,根据平均相对分子质量确定含有甲烷是解题的关键.


科目:高中化学 来源: 题型:解答题
 ,此反应类型为:取代反应.
,此反应类型为:取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 序号 | 金属 质量/g | 金属 状态 | c(H2SO4) mol/L | V(H2SO4) mL | 溶液温度/℃ | 金属消失 的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.7 | 50 | 20 | 35 | 250 |
| 2 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 3 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 4 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
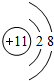
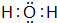 、
、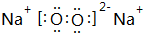 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧燃料电池可将热能直接转变为电能 | |
| B. | 燃料电池的能量转化率可达100% | |
| C. | 氢氧燃料电池工作时氢气在正极被氧化 | |
| D. | 以KOH溶液为电解质溶液的氢氧燃料电池,正极反应为O2+2H2O+4e-=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com