
【题目】在H2SO4、K2SO4、Al2(SO4)3和明矾[KAl(SO4)212H2O]的混合溶液中,H+的浓度为0.2mol/L,SO42﹣的浓度为0.5mol/L,当加入等体积0.6mol/L KOH溶液时,生成的沉淀恰好完全溶解.则反应后溶液中K+的浓度约为( )
A.0.225mol/L
B.0.25mol/L
C.0.45mol/L
D.0.55mol/L
【答案】D
【解析】解:H2SO4、Al2(SO4)3、K2SO4和明矾的混和溶液中,加入等体积的0.6mol/L的KOH溶液时,氢离子优先反应,0.2mol/L的氢离子消耗0.2mol/L的氢氧根离子,则与铝离子反应的氢氧根离子的浓度为:0.6mol/L﹣0.2mol/L=0.4mol/L; 生成的沉淀恰好溶解,发生反应Al3++4OH﹣=AlO2﹣+2H2O,可知原溶液中c(Al3+)= ![]() ×0.4mol/L=0.1mol/L,
×0.4mol/L=0.1mol/L,
根据电荷守恒可知,原溶液中:c(H+)+c(K+)+3c(Al3+)=2c(SO42﹣),即c(K+)=2c(SO42﹣)﹣3c(Al3+)﹣c(H+)=2×0.5mol/L﹣0.1mol/L×3﹣0.2mol/L=0.5mol/L;
设溶液体积为V,反应前后钾离子的物质的量不变,则反应后溶液中K+的浓度约为 ![]() =0.55mol/L,
=0.55mol/L,
故选D.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列关于铝及其化合物叙述中,不正确的是
A. 不能用铝制的器皿来盛放酸梅汤或碱水
B. 铝可作生活用品材质,因铝的化学性质很稳定
C. 氧化铝既可以用来冶炼铝,也可用作耐火材料
D. 铝热反应可用于焊接钢轨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲探究Na2O2与水的反应,可供使用的试剂有:Na2O2、蒸馏水、KMnO4酸性溶液、MnO2 . 该同学取一定量Na2O2样品与过量水反应,待完全反应后,得到溶液X和一定量O2 , 该同学推测反应中可能生成了H2O2 , 并进行实验探究.
(1)写出Na2O2与水反应的化学方程式 .
(2)试设计实验证明溶液X中含过氧化氢 .
(3)通过上述实验证明溶液中确实存在H2O2 . 取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:H2O2+Fe2++OH﹣﹣﹣Fe(OH)3↓,该反应中H2O2表现了性(填“氧化”或“还原”).
(4)已知溶液X可使酸性KMnO4溶液褪色,同时放出氧气,此时H2O2表现了性(填“氧化”或“还原”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向MgSO4和Al2(SO4)3的混合溶液中,逐滴加入NaOH溶液.下列图象中,能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量)( )
A.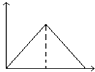
B.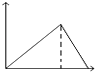
C.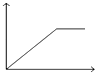
D.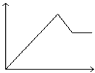
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2mol某烃A在氧气中充分燃烧后,生成化合物B、C各1.2mol.
(1)烃A的分子式为 .
(2)若烃A不能使溴水褪色,但在一定条件下,能与Cl2发生取代反应,其一氯代物只有一种,则A的结构简式为 .
(3)若烃A能使溴水褪色,且所有碳原子都在同一平面内,该物质的结构简式为 .
(4)若某物质A的结构简式如图所示: ![]() 它的同分异构体中不能与金属钠反应生成氢气的共有种(不考虑立体异构),其中核磁共振氢谱只有两组峰,且峰面积比为3:1的为(写结构简式).
它的同分异构体中不能与金属钠反应生成氢气的共有种(不考虑立体异构),其中核磁共振氢谱只有两组峰,且峰面积比为3:1的为(写结构简式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为4种常见溶液中溶质的质量分数和物质的量浓度:
溶质 | HCl | NaOH | CH3COOH | HNO3 |
溶质的质量分数/% | 36.5 | 40 | 60 | 63 |
物质的量浓度/mol·L1 | 11.8 | 14.3 | 10.6 | 13.8 |
这4种溶液中密度最小的是
A.HCl B.NaOH C.CH3COOH D.HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂用软锰矿(含MnO2及少量Al2O3)和闪锌矿(含ZnS及少量FeS)联合生产Zn、MnO2 , 其部分生产流程如下: 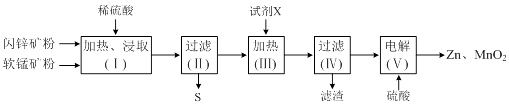
已知:过滤(Ⅱ)所得滤液是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液.相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0molL﹣1计算)如下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Zn(OH)2 | Mn(OH)2 |
开始沉淀时的pH | 2.7 | 4.0 | 6.4 | 7.7 |
完全沉淀时的pH | 3.7 | 5.2 | 8.0 | 10.4 |
(1)加热、浸取时所加矿石均需粉碎,其目的是 .
(2)写出FeS和MnO2和稀硫酸反应的离子方程式: .
(3)试剂X的作用是调节溶液的pH以生成Fe(OH)3、Al(OH)3 . pH调节的范围是 , 试剂X可以选用(填选项字母).
A.MnCO3 B.Na2CO3 C.Zn2(OH)2CO3 D.NH3H2O
(4)电解(Ⅴ)中阳极的电极反应式为 .
(5)Zn和MnO2是制作电池的原料.某锌﹣锰碱性电池以KOH溶液为电解质溶液,其电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s).该电池的正极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列五组物质:A、O2和O3 B、3517Cl和3717Cl C、CH4与C7H16 D、CH3CH2CH2CH3 与 ![]()
(1)组两种物质互为同位素;
(2)组两种物质互为同素异形体;
(3)组两种物质互为同系物;
(4)组两种物质互为同分异构体.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3和NaHCO3是两种常见的钠盐.
(1)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈色.
(2)等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,在相同条件下产生CO2的体积V(Na2CO3) V(NaHCO3)填“大于”,“小于”或“等于”)
(3)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了 2.48g,则原混合物中碳酸钠的质量分数为 .
(4)①实验室中需2mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是 .
A. 1000ml; 212g B.950ml;543.4g C.任意规格; 572g D.500ml; 106g
②需要的玻璃仪器有容量瓶、玻璃棒、烧杯、量筒,还缺少的玻璃仪器有(填写仪器
③名称)若出现如下情况,其中将引起所配溶液浓度偏高的是(填下列编号);
A.容量瓶实验前用蒸馏水洗干净,但未烘干
B.定容观察液面时俯视
C.未冷却至室温就开始定容
D.加蒸馏水时不慎超过了刻度.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com