
分析 在稀NaOH溶液中持续通入CO2气体,当NaOH过量时,二者反应生成碳酸钠和水,如果二氧化碳过量时,碳酸钠和水、二氧化碳反应生成碳酸氢钠.
解答 解:在稀NaOH溶液中持续通入CO2气体,当NaOH过量时,二者反应生成碳酸钠和水,离子方程式为2OH-+CO2=CO32-+H2O;如果二氧化碳过量时,碳酸钠和水、二氧化碳反应生成碳酸氢钠,离子方程式为CO32-+H2O+CO2=2HCO3-,
故答案为:2OH-+CO2=CO32-+H2O;CO32-+H2O+CO2=2HCO3-.
点评 本题考查离子方程式书写,为高频考点,明确产物成分是解本题关键,注意碳酸根离子能与二氧化碳、水反应,注意该反应产物与反应物的量有关,题目难度不大.


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,18 g H2O中含有的质子数为10 NA | |
| B. | 标准状况下,2.24 L Cl2通入水中,反应转移的电子数为0.1 NA | |
| C. | 常温常压下,53.5 g NH4Cl晶体中含有共价键的数目为4 NA | |
| D. | 常温常压下,2 L 0.5 mol•L-1 硫酸钾溶液中阴、阳离子总数大于3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 理论上任何一个自发的氧化还原反应均可以设计成原电池,根据氧化还原反应:Fe+2Fe3+=2Fe2+设计的原电池如图所示,其中盐桥内盛装有含KNO3饱和溶液的琼脂.
理论上任何一个自发的氧化还原反应均可以设计成原电池,根据氧化还原反应:Fe+2Fe3+=2Fe2+设计的原电池如图所示,其中盐桥内盛装有含KNO3饱和溶液的琼脂.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将氢氧化钠固体放在滤纸上称量 | |
| B. | 用10 mL量筒量取8.58 mL蒸馏水 | |
| C. | 配制5%的食盐溶液时,将称量好的食盐放入烧杯中加适量的水搅拌溶解 | |
| D. | 稀释浓硫酸溶液时,将量取的浓硫酸放入烧杯中加水稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2是氧化剂,NaOH是还原剂 | |
| B. | 被氧化的氯原子个数与被还原的氯原子个数比是1:5 | |
| C. | Cl2既是氧化剂,又是还原剂 | |
| D. | 得电子的氯原子个数与失电子的氯原子个数之比为5:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中氮元素被氧化 | |
| B. | 该反应中H2O2作还原剂 | |
| C. | 0.1mol•L-1NaCN溶液中含有HCN和CN-的总数为0.1×6.02×1023 | |
| D. | 实验室配制NaCN溶液时,需加入适量的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
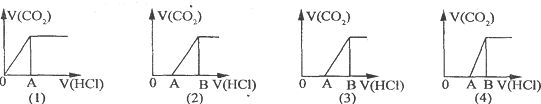
| A. | (1)图显示M中只有一种溶质且为Na2CO3 | |
| B. | (3)图显示M中有两种溶质且为Na2CO3.NaOH | |
| C. | (2)图显示M中有两种溶质且为Na2CO3.NaHCO3 | |
| D. | (4)图显示M中c(NaHCO3)=c(Na2CO3) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com