
����Ŀ����������̼���º���{[Ni��CHZ��3]��ClO4��2 }��һ�����͵���ҩ��
��1��Ni2+��̬��������Ų�ʽΪ ��
��2��ClO4���Ŀռ乹��������ClO4����Ϊ�ȵ������һ�ַ���Ϊ���ѧʽ����
��3����ѧʽ��CHZΪ̼���£����ΪCO��N2H3��2 �� ̼������̼ԭ�ӵ��ӻ��������Ϊ��1molCO��N2H3��2�����к��ЦҼ���ĿΪ ��
��4����������̼���º�������NiO�������ἰ̼���»��϶��ɣ�NiO�ľ����ṹ��ͼ��ʾ�������к��е�Ni2+��ĿΪa��Ni2+����λ��Ϊb��NiO������ÿ�������Ӿ����������������ĿΪc����a��b��c= �� 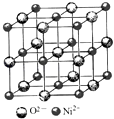
���𰸡�
��1��1s22s22p63s23p63d8
��2���������壻CCl4��
��3��sp2��11��6.02��1023
��4��2��3��6
���������⣺��1��NiԪ��ԭ�Ӻ�����28�����ӣ�ԭ�Ӻ�������Ų�Ϊ1s22s22p63s23p63d84s2 �� Niʧȥ4s�ܼ�2�������γ�Ni2+ �� Ni2+���Ӻ�������Ų�ʽΪ��1s22s22p63s23p63d8 �� ���Դ��ǣ�1s22s22p63s23p63d8����2��ClO4������ԭ�Ӽ۲���Ӷ���Ϊ4+ ![]() =4��û�йµ��Ӷԣ�����ռ乹���ǣ��������壻ԭ��������ͬ���۵���������ͬ������Ϊ�ȵ����壬��ClO4����Ϊ�ȵ������һ�ַ���ΪCCl4�ȣ����Դ��ǣ��������壻CCl4�ȣ���3��CO��N2H3��2��Cԭ����Oԭ��֮���γ�˫������Nԭ��֮���γ�C��N������û�й¶Ե��ӣ��ӻ������ĿΪ3��Cԭ�Ӳ�ȡsp2�ӻ�����N2H3�е�ԭ��֮���γ�N��N������Nԭ����Hԭ��֮���γ�N��H�����������к���11���Ҽ�����1molCO��N2H3��2�����к��ЦҼ���ĿΪ11��6.02��1023 �� ���Դ��ǣ�sp2��11��6.02��1023����4����Ni2+����λ�ھ������㼰���ģ�������Ni2+��Ŀx=8��
=4��û�йµ��Ӷԣ�����ռ乹���ǣ��������壻ԭ��������ͬ���۵���������ͬ������Ϊ�ȵ����壬��ClO4����Ϊ�ȵ������һ�ַ���ΪCCl4�ȣ����Դ��ǣ��������壻CCl4�ȣ���3��CO��N2H3��2��Cԭ����Oԭ��֮���γ�˫������Nԭ��֮���γ�C��N������û�й¶Ե��ӣ��ӻ������ĿΪ3��Cԭ�Ӳ�ȡsp2�ӻ�����N2H3�е�ԭ��֮���γ�N��N������Nԭ����Hԭ��֮���γ�N��H�����������к���11���Ҽ�����1molCO��N2H3��2�����к��ЦҼ���ĿΪ11��6.02��1023 �� ���Դ��ǣ�sp2��11��6.02��1023����4����Ni2+����λ�ھ������㼰���ģ�������Ni2+��Ŀx=8�� ![]() +6��
+6�� ![]() =4���Զ���Ni2+�����о�����֮�����O2������λ�����м��ҹ���Ni2+���ӶԳƣ���Ni2+����λ��y=6����֮�����Ni2+����λ�����ģ�ÿ������Ϊ12���湲�ã���֮�����������������Ŀz=12����x��y��z=4��6��12=2��3��6�����Դ��ǣ�2��3��6��
=4���Զ���Ni2+�����о�����֮�����O2������λ�����м��ҹ���Ni2+���ӶԳƣ���Ni2+����λ��y=6����֮�����Ni2+����λ�����ģ�ÿ������Ϊ12���湲�ã���֮�����������������Ŀz=12����x��y��z=4��6��12=2��3��6�����Դ��ǣ�2��3��6��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� ��һ��ҽѧ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳɣ�
��һ��ҽѧ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳɣ� 
�ش��������⣺
��1��A��������������ͭ������Ӧ����ש��ɫ������A�Ľṹ��ʽ�� ��
��2��B�ĺ��������ŵ������� �� C+E��F�ķ�Ӧ������ ��
��3��F�ķ���ʽ�� �� �÷��ӵ�����ʺɱ�Ϊ ��
��4�����������������л����ͬ���칹�����֣���д��һ�ֵĽṹ��ʽa����F��Ϊͬ���칹��b��������c�����ڶ�Ԫ����d��������ֻ��һ��ȡ����
��5��д��G����NaOH��Һ����ʱ��Ӧ�Ļ�ѧ����ʽ��
��6�����й����������ʵ�������ȷ����������ţ�����1molD����2molNaHCO3��Һ��Ӧ
��E����FeCl3��Һ������ɫ��Ӧ
��B���������������ܸ��ݺ˴Ź�������������
��1molG�������5molH2�����ӳɷ�Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��װ�ý��е�ʵ�飬�ܴﵽ��Ӧʵ��Ŀ���ǣ� �� 
A.װ�üף��ռ�NO2����
B.װ���ң���֤X��ҺΪŨ����
C.װ�ñ�����֤������ˮ�е��ܽ���
D.װ�ö�����������β��NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڰ��˻��ϱ����ã���ṹ��ʽ����ͼ��ʾ������������ȷ������ ��

A. ����������������������ķ���ʽ��C14H14Cl2O4
B. ����������ڴ���ͬһƽ���ԭ�Ӳ�����10��
C. 1 mol����������7 mol H2�����ӳɷ�Ӧ
D. ����������FeCl3��Һ������ɫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Լ���Ϊȼ�ϵ����͵�أ���ɱ�����������Ϊȼ�ϵĴ�ͳȼ�ϵ�أ�Ŀǰ�õ��㷺���о�����ͼ��Ŀǰ�о��϶��һ�����������ȼ�ϵ�ع���ԭ��ʾ��ͼ���ش��������⣺
��1��B���ϵĵ缫��ӦʽΪ
��2�����ø�ȼ�ϵ������Դ����ʯī���缫���100mL 1mol/L������ͭ��Һ���������ռ���������������ʱ�����������ĵļ�������Ϊ������£���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NaOH��Na2O2��ɵĻ��������Ԫ�ص���������Ϊ58��������������Ԫ�ص���������Ϊ�� ��
A. 62% B. 2% C. 4% D. ��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���� ( )
A. ú�����л�������
B. �����ʱ仯�����ϣ�ú�ĸ�����̰����������仯�ͻ�ѧ�仯
C. ú�к��д����ı��ȷ�������ú�Ƿ���������Ҫ��Դ
D. ˮú����ͨ��ú��Һ���õ�������ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������������ֱ�ͨ����ʼ�����ͬ���ܱ�������͢��У�ʹ�䷢����Ӧ��t0ʱ�������дﵽ��ѧƽ�⣬X,Y,Z�����ʵ����ı仯��ͼ��ʾ���������й��ƶ���ȷ���� �� �� 
A.�÷�Ӧ�Ļ�ѧ����ʽΪ3X+2Y2Z
B.���������о��ﵽƽ��ʱ�������������V����V������������ﵽƽ������ʱ�����t0
C.���������о��ﵽƽ��ʱ����������Z�����ʵ���������ͬ����YΪ��̬��Һ̬
D.����ƽ��������������¶�ʱ���������˵��Z�����ķ�ӦΪ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com