
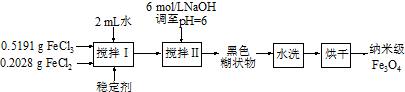
分析 (1)依据流程图分析制备反应过程,是氯化铁、氯化亚铁在氢氧化钠溶液中生成四氧化三铁、水、氯化钠;根据电荷守恒可写出该方程式;
(2)反应条件温度低于100°C,需要用水浴加热,水浴加热温度容易控制,加热均匀;
(3)分离固体和液体通常用过滤操作;
(4)水洗的主要作用是洗去吸附在黑色糊状物表面的Fe3+和Cl-,只要检验其中一个不存在即可;
(5)Fe3O4达到纳米级,即在溶液形成胶体,利用胶体的丁达尔效应证明Fe3O4达到纳米级;
解答 解:(1)由流程可知,生成Fe3O4的反应物为Fe2+、Fe3+和OH-,根据电荷守恒可写出该方程式为:Fe2++2Fe3++8OH-=Fe3O4+4H2O,
故答案为:Fe2++2Fe3++8OH-=Fe3O4+4H2O;
(2)低于100℃的温度控制通常用水浴加热法,故选B;
(3)分离固体和液体通常用过滤操作,从黑色糊状物的悬浊液中分离出Fe3O4的实验操作是过滤;
故答案为:过滤;
(4)水洗的主要作用是洗去吸附在黑色糊状物表面的Fe3+和Cl-,只要检验其中一个不存在即可,取最后的倾出液,取少量最后的倾出液于试管中,滴加几滴KSCN溶液,溶液不变血红色则已洗净(或取少量最后的倾出液于试管中,滴加几滴经稀硝酸酸化的硝酸银溶液,不产生沉淀则已洗净.),
故答案为:取最后的倾出液,取少量最后的倾出液于试管中,滴加几滴KSCN溶液,溶液不变血红色则已洗净(或取少量最后的倾出液于试管中,滴加几滴经稀硝酸酸化的硝酸银溶液,不产生沉淀则已洗净.);
(5)Fe3O4达到纳米级,即在溶液形成胶体,利用胶体的丁达尔效应证明Fe3O4达到纳米级,即做丁达尔效应实验(用一支激光笔照射所得产物,如有一条光亮的通路,证明已达纳米级),
故答案为:做丁达尔效应实验(用一支激光笔照射所得产物,如有一条光亮的通路,证明已达纳米级).
点评 本题考查了制备实验的设计,流程分析判断,反应条件的应用,实验基本操作的迁移应用能力,解答此类题的关键是一定要注意题中所给的信息,题目难度中等.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | Cl2是氧化剂,NaOH是还原剂 | |
| B. | 被氧化的Cl原子和被还原的Cl原子的物质的量的比为5:1 | |
| C. | 每生成1mol的NaClO3转移6mol的电子 | |
| D. | Cl2既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15 种 | B. | 16 种 | C. | 17 种 | D. | 18 种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L由H2和O2组成的混合气体,所含分子总数为NA | |
| B. | 1mol Cl2参加反应,转移的电子数一定为2NA | |
| C. | 常温常压下,1 mol氖气含有的原子数为NA | |
| D. | 1L1 mol.L-l FeCl3溶液中Fe3+的数目小于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,电池的负极反应为LiC6-e-═Li++C6 | |
| B. | 充电时,电池的正极反应为CoO2+Li++e-═LiCoO2 | |
| C. | 羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质 | |
| D. | 锂离子电池的比能量(单位质量释放的能量)低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com