

���� C��Ũ���ᷴӦ����ʽΪC+2H2SO4��Ũ�� $\frac{\underline{\;\;��\;\;}}{\;}$CO2��+2SO2��+2H2O���÷�Ӧ������CO2��SO2�����������嶼��ʹ����ʯ��ˮ����ǣ��������������Ư���ԡ���ԭ�ԣ�������ʹƷ����Һ��ɫ���ܱ����Ը�������������÷�Ӧ��Ũ���������������ݴ˷������
��� �⣺��1��C��Ũ���ᷴӦ����ʽΪC+2H2SO4��Ũ�� $\frac{\underline{\;\;��\;\;}}{\;}$CO2��+2SO2��+2H2O���÷�Ӧ��SԪ�ػ��ϼ���+6�۱�Ϊ+4�ۣ�����Ũ��������������
�ʴ�Ϊ����������
��2��SO2����Ư���ԣ���ʹƷ����Һ��ɫ��
�ʴ�Ϊ��Ư�ף�
��3������������л�ԭ�ԣ��ܱ����Ը����������������ϴ��ƿ���е������Ǹ��������Һ��ɫ��
�ʴ�Ϊ�����������Һ��ɫ��
��4��CO2��SO2���������嶼��ʹ����ʯ��ˮ����ǣ��������������Ư���ԡ���ԭ�ԣ�������ʹƷ����Һ��ɫ���ܱ����Ը���������������Խ��������ͨ���һ��ϴ��ƿ�м����������ͨ��ڶ���ϴ��ƿ�г�ȥ��������ͨ�������ϴ��ƿ���ų���������Ĵ��ڣ���ϴ��ƿ�۵������Ǽ�����������Ƿ������
�ʴ�Ϊ��������������Ƿ������
��5��ϴ��ƿ������ҺΪ����ʯ��ˮ����������Ǽ��������̼����ʯ��ˮ����ǣ�˵���ж�����̼��
�ʴ�Ϊ�����������̼��
���� ������Ũ�����̼�ķ�ӦΪ���忼�����ʵļ��飬��ȷ���ʵ������ǽⱾ��ؼ�������CO2��SO2�������������ʵ������ԺͲ��������ʵ�鼴�ɣ�֪���������ʵļ��鷽������Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ�䣨s�� | 0 | 4 | 8 | 12 | 16 | 20 |
| n��N2O4����mol�� | 0.40 | a | 0.20 | c | d | e |
| n��NO2����mol�� | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������� | ϩ�� | �� | ȩ | ���������� |
| ���������� | ̼̼˫�� | �ǻ� | ȩ�� | ���� |
| �ṹ��ʽ |  | -OH | -CHO | -NO2 |
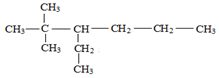 ������Ϊ2��2-����-3-�һ����飮
������Ϊ2��2-����-3-�һ����飮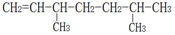 ������Ϊ2��5-����-1-��ϩ��
������Ϊ2��5-����-1-��ϩ��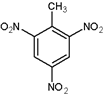 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��Fe3+��=0.1 mol/L��Һ�У�Na+��NH4+��SCN-��SO42- | |
| B�� | ���ܽ�CaCO3����Һ�У�Fe3+��Ca2+��Cl-��NO3- | |
| C�� | ��ˮ�������c��H+��=1��10-2mol/L����Һ�У�Na+��Ba2+��HCO3-��Cl- | |
| D�� | ǿ������Һ�У�K+��Na+��ClO-��I- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
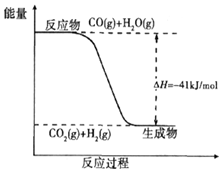 ú̿����ת��Ϊ�����Դ�ͻ���ԭ�ϣ�
ú̿����ת��Ϊ�����Դ�ͻ���ԭ�ϣ��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com