
【题目】在25℃时,对于0.1molL﹣1的氨水,请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中 ![]() 将(填“增大”、“减小”或“不变”);
将(填“增大”、“减小”或“不变”);
(2)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,此时溶液的pH7(填“大于”、“小于”或“等于”),用离子方程式表示其原因 , 此时溶液中各离子浓度由大到小的顺序为 .
(3)若向氨水中加入0.05molL﹣1稀硫酸至溶液正好呈中性,所用氨水的体积V1与稀硫酸的体积V2的关系为V1V2(填“大于”、“小于”或“等于”),写出溶液中各离子浓度之间满足的电荷守恒表达式 .
【答案】
(1)增大
(2)小于;NH4++H2O ![]() NH3?H2O+H+;c(NH4+)>c(SO42﹣ )>c(H+)>c(OH﹣)
NH3?H2O+H+;c(NH4+)>c(SO42﹣ )>c(H+)>c(OH﹣)
(3)大于;c(NH4+)+c(H+)=2c(SO42﹣ )+c(OH﹣)
【解析】解:(1)由于(NH4)2SO4=2NH4++SO42﹣ , 溶液中NH4+浓度增大,所以答案是:增大.(2)pH=1的硫酸溶液,C( H +)=0.1molL﹣1 , 氢离子浓度与氨水浓度相等,体积相同,所以恰好反应生成盐,但由于硫酸铵是强酸弱碱盐,铵根离子水解,使溶液呈酸性,PH<7;如果NH4+不水解,C( NH4+):C(SO42﹣)=2:1,但水解是较弱的,所以c(NH4+)>c(SO42﹣ );溶液呈酸性,所以c(H+)>c(OH﹣);
所以答案是:小于;NH4++H2O ![]() NH3H2O+H+;c(NH4+)>c(SO42﹣ )>c(H+)>c(OH﹣);(3)酸碱浓度比为1:2,由H2SO4+2NH3 . H2O=(NH4)2SO4+2H20得,酸碱溶液的体积比应为1:1,但由于硫酸铵是强酸弱碱盐,铵根离子水解,使溶液呈酸性,要想使溶液呈中性,加入碱液的体积要比恰好反应的大一些;无论溶液的酸碱性如何,但溶液中阴阳离子所带电荷相等,即c(NH4+)V×NA×1+c(H+)V×NA×1=c(SO42﹣ )V×NA×2+c(OH﹣)V×NA×1,化简得c(NH4+)+c(H+)=2c(SO42﹣ )+c(OH﹣)
NH3H2O+H+;c(NH4+)>c(SO42﹣ )>c(H+)>c(OH﹣);(3)酸碱浓度比为1:2,由H2SO4+2NH3 . H2O=(NH4)2SO4+2H20得,酸碱溶液的体积比应为1:1,但由于硫酸铵是强酸弱碱盐,铵根离子水解,使溶液呈酸性,要想使溶液呈中性,加入碱液的体积要比恰好反应的大一些;无论溶液的酸碱性如何,但溶液中阴阳离子所带电荷相等,即c(NH4+)V×NA×1+c(H+)V×NA×1=c(SO42﹣ )V×NA×2+c(OH﹣)V×NA×1,化简得c(NH4+)+c(H+)=2c(SO42﹣ )+c(OH﹣)
所以答案是:大于;c(NH4+)+c(H+)=2c(SO42﹣ )+c(OH﹣).
【考点精析】利用弱电解质在水溶液中的电离平衡对题目进行判断即可得到答案,需要熟知当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】一定条件下的2L密闭容器,进行反应2X(g)+Y(g)2Z(g),若起始时X、Y、Z物质的量分别为n1、n2、n3(均不为零).达平衡时,X、Y、Z浓度分别为0.2mol/L、0.1mol/L和0.08mol/L,则下列判断合理的是( )
A.X和Y的转化率不一定相等
B.n1、n2=2:1
C.平衡时,Y和Z的生成速率之比为2:1
D.n,的取值范围为0<n1<0.28
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电离度是描述弱电解质电离程度的物理量,电离度=(已电离的电解质的物质的量/原来总的物质的量)×100%.现取20mL pH=3的 CH3COOH溶液,加入0.2molL﹣1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为( ) 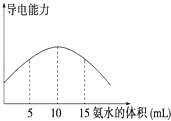
A.0.5%
B.1.5%
C.0.1%
D.1%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲使醋酸溶液中的CH3COO﹣浓度增大,电离平衡向右移动,且不放出气体,可向醋酸溶液中加入少量固体( )
A.NaOH
B.NaHCO3
C.CH3COOK
D.Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡.
请根据所学知识的回答:
(1)浓度为0.1mol/L的8种溶液:①HNO3 ②H2SO4③HCOOH ④Ba(OH)2⑤NaOH ⑥CH3COONa ⑦KCl ⑧NH4Cl 溶液pH值由小到大的顺序是(填写编号) .
(2)B为0.1molL﹣1NaHCO3溶液,实验测得NaHCO3溶液的pH>7,请用离子方程式表示其原因: .
(3)在0.10molL﹣1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=(已知Ksp[Cu(OH)2]=2.2x10﹣20).若在0.10molL﹣1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是制取无水氯化铁的实验装置图。请回答下列问题:
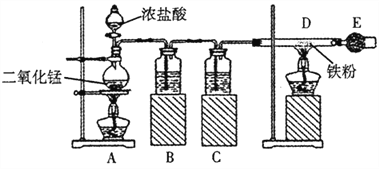
已知:氯化铁易潮解。
(1)烧瓶中发生反应的化学方程式是_________________;
(2)B瓶中的溶液是_________________,C瓶中溶液的作用是_________________。
(3)干燥管E中盛有碱石灰,其作用是_________________。
(4)开始实验时,应先点燃_________________(填字母)处的酒精灯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能在溶液中大量共存的是( )
A.Na+、Mg2+、OH-、Br-B.H+、Fe2+、SO42-、NO3-
C.K+、NH4+、CO32-、OH-D.Ca2+、Al3+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将SO2分别通入下列4种溶液中,有关说法不正确的是( )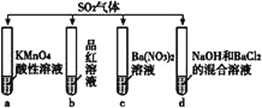
A. 试管a中实验可以证明SO2具有还原性 B. 试管b中溶液褪色,说明SO2具有漂白性
C. 试管c中能产生白色沉淀,说明SO2具有氧化性 D. 试管d中能产生白色沉淀,该沉淀不溶于稀硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com