
| ||
| ||


 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:
| A、5L Cl2与5L HCl |
| B、0.2molO2与标准状况下的22.4L酒精 |
| C、36gH2O与通常状况下44.8L CO2 |
| D、25°C,101kPa时,等体积的空气与H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 高铁酸钾是20世纪70年代以来开发的一种继臭氧、过氧化氢、二氧化氯之后一种新型水处理剂,它能快速杀灭水中的细菌和病毒,且不会生成三氯甲烷、氯代酚等次级衍生物.高铁酸根(FeO42-)在溶液中呈紫红色,溶液的pH对高铁酸根稳定性的影响很大,当pH值为10~11时非常稳定,而当pH<7.5时,稳定性明显下降,分解放出氧气,并析出具有高度吸附活性的无机絮凝剂Fe(OH)3.电解法制备高铁酸钾原理如图所示.
高铁酸钾是20世纪70年代以来开发的一种继臭氧、过氧化氢、二氧化氯之后一种新型水处理剂,它能快速杀灭水中的细菌和病毒,且不会生成三氯甲烷、氯代酚等次级衍生物.高铁酸根(FeO42-)在溶液中呈紫红色,溶液的pH对高铁酸根稳定性的影响很大,当pH值为10~11时非常稳定,而当pH<7.5时,稳定性明显下降,分解放出氧气,并析出具有高度吸附活性的无机絮凝剂Fe(OH)3.电解法制备高铁酸钾原理如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
 已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.
已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
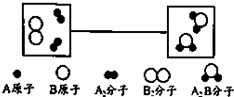
| A、原子是化学变化中的最小粒子 |
| B、元素的种类、原子的数目在化学反应前后不变 |
| C、在化学变化中分子分成原子,原子又重新组合成新物质的分子 |
| D、上述反应的化学方程式可表示为:2A+B=A2B |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加催化剂,V正、V逆 都发生变化,且变化的倍数相等 |
| B、加压,V正、V逆 都增大,且V正 增大的倍数大于V逆增大的倍数 |
| C、降温,V正、V逆 都减小,且V正 减小的倍数大于V逆减小的倍数 |
| D、增大氮气的浓度,V正、V逆 都增大,且V正 增大倍数大于V逆 增大倍数;化学平衡正移,N2 转换率增大,H2转化率也增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质的量都是1mol |
| B、质量相同 |
| C、含有的氧原子个数相同 |
| D、两者的密度相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com