
分析 (1)①高炉炼铁的原料:铁矿石、焦炭、石灰石;制普通玻璃的原料:石英砂、石灰石、纯碱等;在炼铁高炉中,焦炭在空气中燃烧生成二氧化碳,生成的二氧化碳在高温条件下与焦炭发生反应生成一氧化碳,在高温下氧化铁和一氧化碳反应生成铁和二氧化碳;
②铝的密度小,表面容易形成致密的氧化膜,抗腐蚀性能好,与浓硫酸发生钝化反应;
③单质是由一种元素组成的纯净物,化合物是由不同种元素组成的纯净物;纯净物由一种物质组成,混合物由两种或两种以上的物质组成;
(2)①容量瓶带有瓶塞,使用过程中需要上下颠倒,此操作要求容量瓶不能漏水;根据m=cVM计算出碳酸钠的质量;
②加水至离刻度线1~2cm时,改用胶头滴管滴加水至液面与刻度线相切;
③根据c=$\frac{n}{V}$,通过判断不当操作对溶质的物质的量n和溶液体积V的影响来分析误差;
④碳酸钠和盐酸反应生成氯化钠、水以及二氧化碳,稀释前后反应本质相同;
(3)①SO2气体溶于水后生成H2SO3,H2SO3随雨水的下降,逐渐被空气中的氧气所氧化生成易电离的H2SO4,从而使雨水的酸性增强;在已经酸化的土壤中加石灰,可以改良土壤;
②大量的氮氧化物排放到空气中,会形成硝酸型酸雨,氮氧化物可用氢氧化钠溶液吸收,转化为NaNO3、NaNO2、H2O,汽车安装尾气催化转化装置,可将尾气中的氮氧化物和一氧化碳反应,转化为二氧化碳和氮气.
解答 解:(1)①高炉炼铁的原料:铁矿石、焦炭、石灰石;制普通玻璃的原料:石英砂、石灰石、纯碱,所以高炉炼铁和普通玻璃都要用到的原料是石灰石,在炼铁高炉中,焦炭在空气中燃烧生成二氧化碳,生成的二氧化碳在高温条件下与焦炭发生反应生成一氧化碳,在高温下氧化铁和一氧化碳反应生成铁和二氧化碳,发生的一系列反应为C+O2 $\frac{\underline{\;点燃\;}}{\;}$CO2,CO2+C $\frac{\underline{\;高温\;}}{\;}$2CO,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,所以将铁矿石还原成单质的还原剂是CO,
故答案为:石灰石;CO;
②铝密度小,铝的表面容易被氧化生成氧化铝,为致密的氧化膜结构,所以抗腐蚀性能好,与浓硫酸反应发生钝化反应,为致密的氧化膜结构,不是不反应,故C错误;
故答案为:C;
③钢铁、铝合金都属于金属合金,属于混合物,玻璃主要成分为硅酸钠、二氧化硅、硅酸钙等为主的硅酸盐材料,三者都属于混合物,
故答案为:a;
(2)①容量瓶带有瓶塞,使用过程中需要上下颠倒,此操作要求容量瓶不能漏水,所以容量瓶在使用前需要检查是否漏水;欲配制0.2mol/LNa2CO3溶液100mL,需要碳酸钠的质量为:0.1L×0.2mol/L×106g/mol=2.12g;
故答案为:检查是否漏水;2.12;
②操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取(用到胶头滴管),在烧杯中稀释,用玻璃棒搅拌,冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,故摇匀前的一步操作是定容,
故答案为:定容;
③a.定容时俯视刻度线,会导致溶液体积偏小,则浓度偏大,故a错误;
b.定容时,如果加水超过了刻度线,立即用胶头滴管吸出多余的部分,多余的部分含有溶质,溶质质量偏小,则配制出的溶液的浓度偏小,故b正确;
c.将称出的Na2CO3在烧杯中溶解,所得溶液恢复至室温再转移到容量瓶中,操作正确,对浓度无影响,故C错误;
故答案为:b;
④碳酸钠和盐酸反应生成氯化钠、水以及二氧化碳,稀释前后碳酸钠的物质的量不变,本质都为CO32-+2H+=CO2↑+H2O,所以两者消耗的盐酸的量相同,
故答案为:相同;
(3)①SO2气体溶于水后生成H2SO3,H2SO3随雨水的下降,逐渐被空气中的氧气所氧化生成易电离的H2SO4,2H2SO3+O2=2H2SO4,从而使雨水的酸性增强,酸性土壤加入碱性物质进行中和,在已经酸化的土壤中加石灰,可以改良土壤,
故答案为:2H2SO3+O2=2H2SO4;石灰;
②大量的氮氧化物排放到空气中,会形成硝酸型酸雨,氮氧化物可用氢氧化钠溶液吸收,反应为:NO+NO2+2NaOH═2NaNO2+H2O,2NO2+2NaOH═NaNO2+NaNO3+H2O,
转化为NaNO3、NaNO2、H2O,汽车安装尾气催化转化装置,可将尾气中的氮氧化物和一氧化碳反应:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2,转化为二氧化碳和氮气,
故答案为:NaNO2;N2.
点评 本题考查化学与生活、溶液的配制等知识,掌握氮、硫以及实验基本操作是解答关键,题目难度中等.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:解答题
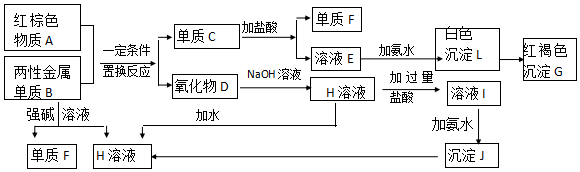
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氯有酸性,氯水也有酸性 | |
| B. | 液氯和氯水都有漂白性 | |
| C. | 液氯是纯净物,而氯水是混合物 | |
| D. | 液氯无色,氯水呈黄绿色,两者均存在氯离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 实验内容 | 实验目的 |
| A. | 用pH试纸测定相同浓度的CH3COONa溶液和NaHCO3溶液的pH | 比较CH3COOH和H2CO3的酸性强弱 |
| B. | 向AgCl浊液中滴加少量的0.1mol•L-1Na2S溶液 | 比较AgCl和Ag2S的溶度积大小 |
| C. | 向1 mol•L-1的稀硫酸中加入ag锌粉,向4 mol•L-1的稀硫酸的中加入ag锌粒 | 探究固体表面积对Zn与稀硫酸反应速率的影响 |
| D. | 将两个完全相同且充满NO2气体的密闭烧瓶分别浸在热水和冰水中 | 探究温度对化学平衡的影响 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用胶头滴管加液时,一般不能伸入试管中 | |
| B. | 蒸馏时一般需在瓶内放一些碎瓷片 | |
| C. | 温度计插入液体中测量温度的同时,又用它搅拌液体 | |
| D. | 用10 mL的量筒可量取5.4mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HS-+H2O?H3O++S2- | B. | CO2+2 H2O?HCO3-+H3O+ | ||
| C. | NH4++2H2O?NH3•H2O+H3O+ | D. | HCO3-+OH-?CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸的电离方程式:H2CO3?2H++CO32- | |
| B. | 碱性氢氧燃料电池负极的电极反应式:H2-2e-=2H+ | |
| C. | HCO3-的水解方程式:HCO3-+H2O?CO32-+H3O+ | |
| D. | 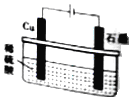 如图所示,反应开始时的离子方程式:Cu+2H+$\frac{\underline{\;通电\;}}{\;}$Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
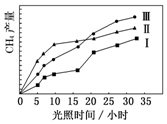 利用光能和光催化剂,可将 CO2 和 H2O(g)转化为 CH4 和 O2.紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示.
利用光能和光催化剂,可将 CO2 和 H2O(g)转化为 CH4 和 O2.紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com