
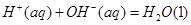
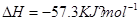
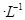 的氢氟酸与0.1mol/L
的氢氟酸与0.1mol/L 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Q1=Q2=Q3 | B.Q2>Q1>Q3 | C.Q2>Q3>Q1 | D.Q2=Q3>Q1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
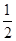 O2(g)=== ZnO(s),ΔH=" -348.3" kJ·mol-1,
O2(g)=== ZnO(s),ΔH=" -348.3" kJ·mol-1,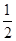 O2(g)=== Ag2O(s),ΔH=" -31.0" kJ·mol-1,则Zn(s)+ Ag2O(s) === ZnO(s)+ 2Ag(s)的ΔH等于( )
O2(g)=== Ag2O(s),ΔH=" -31.0" kJ·mol-1,则Zn(s)+ Ag2O(s) === ZnO(s)+ 2Ag(s)的ΔH等于( )| A.-317.3 kJ·mol-1 | B.-379.3 kJ·mol-1 | C.-332.8 kJ·mol-1 | D.317.3 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C + H2O ="=" CO + H2ΔH= +131.28kJ·mol-1 |
| B.C(s)+ H2O(g) ="=" CO(g) + H2(g)ΔH= +10.94 kJ·mol-1 |
| C.C(s)+ H2O(l) ="=" CO(g) + H2(g)ΔH= +131.28kJ·mol-1 |
| D.C(s)+ H2O(g) ="=" CO(g) + H2(g)ΔH= +131.28kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.350KJ | B.700KJ | C.200KJ | D.250KJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com