
【题目】在下列曲线中,纵坐标表示生成Al(OH)3的质量,横坐标表示加入试剂的体积。下列叙述中不正确的是( )
A. 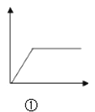 图①可表示向NH3·H2O中滴加AlCl3溶液至过量
图①可表示向NH3·H2O中滴加AlCl3溶液至过量
B. 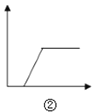 图②可表示向NaOH与NaAlO2的混合溶液中通入CO2至过量
图②可表示向NaOH与NaAlO2的混合溶液中通入CO2至过量
C. 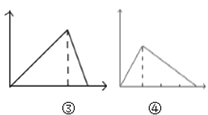 图③可表示向NaOH与NaAlO2的混合液中滴加HCl溶液至过量;而图④可表示向盐酸酸化的AlCl3溶液中滴加NaOH至过量
图③可表示向NaOH与NaAlO2的混合液中滴加HCl溶液至过量;而图④可表示向盐酸酸化的AlCl3溶液中滴加NaOH至过量
D. 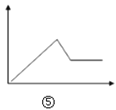 图⑤可表示向MgCl2和AlCl3的混合液中滴加NaOH溶液至过量
图⑤可表示向MgCl2和AlCl3的混合液中滴加NaOH溶液至过量
【答案】C
【解析】
A、NH3·H2O是弱碱,不能溶解氢氧化铝,向NH3·H2O中滴加AlCl3溶液至过量:AlCl3+3NH3H2O=Al(OH)3↓+3NH4Cl,对照图象应为①,A正确;
B、向NaOH与NaAlO2的混合溶液中通入CO2气体:先发生2NaOH+CO2=2H2O+Na2CO3;后逐渐产生沉淀,NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,对照图象应为②,B正确;
C、向NaOH与NaAlO2的混合液中滴加HCl溶液至过量,盐酸首先中和氢氧化钠,然后开始产生氢氧化铝沉淀,盐酸过量后沉淀溶解,图像均不满足;向盐酸酸化的AlCl3溶液中滴加NaOH至过量,氢氧化钠首先中和盐酸,然后沉淀铝离子产生氢氧化铝沉淀,过量后沉淀又溶解,图像均不满足,C错误;
D、向MgCl2和AlCl3的混合液中滴加NaOH溶液至过量,先是生成氢氧化镁和氢氧化铝沉淀,后是氢氧化铝溶解,对照图象应为⑤,D正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B. 1molNa2O2与足量CO2充分反应,转移的电子数为2 NA
C. 25℃1LpH=12的Na2CO3溶液中,由水电离出H+的数目为0.01NA
D. 0.1molH2和0.1molI2于密闭容器中充分反应后,HI分子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路、陶瓷等生产领域。工业上由氧化铝与焦炭在氮气流中高温制得:Al2O3+3C+N2![]() 2AlN+3CO。请回答:
2AlN+3CO。请回答:
(1)上述反应中氧化剂与还原剂的物质的量之比___________________。
(2)制得的氮化铝产品中常含有Al4C3、Al2O3和C等杂质,已知:
稀硫酸(过量) | 浓NaOH溶液(过量) | |
AlN | 2AlN+4H2SO4=Al2(SO4)3+(NH4)2SO4 | AlN+NaOH+H2O=NaAlO2+NH3 ↑ |
Al4C3 | Al4C3+6H2SO4=2Al2(SO4)3+3CH4 ↑ | Al4C3+4NaOH+4H2O=4NaAlO2+3CH4 ↑ |
为测定产品中AlN和Al4C3的含量,设计了如下两套实验装置(在通风橱进行,可适当微热,忽略空气中水蒸气、CO2的影响及NH3在强碱性溶液中的溶解)。

装置I、II在反应前后的质量差分别为m1 g和m2 g,则m g产品中AlN的质量分数为______(用含m、m1、m2的代数式表示)。
(3)取装置I中反应后的滤液,先加入少量(NH4)2SO4溶液,然后依次进行蒸发浓缩、冷却结晶、过滤、用少量酒精洗涤、滤纸吸干,得到铵明矾晶体[NH4Al(SO4)2·12H2O]。
①蒸发浓缩操作时,除需铁架台(带铁圈)、酒精灯、坩埚钳、玻璃棒外,还需要_______(填仪器名称);蒸发浓缩的操作;小火加热,不断搅拌,_________。
②用少量酒精洗涤的目的__________________________。
(4)已知:25℃时,Kw=1.0×10-14,Kb(NH3·H2O)=1.8×10-5,Kb(Al(OH)3]=1.4×10-9。
① NH4Al(SO4)2溶液中离子浓度由大到小的顺序_________________。
②(NH4)2SO4溶液中存在水解平衡,则水解平衡常数为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在催化剂作用下,用乙醇制乙烯,乙醇转化率和乙烯选择性(生成乙烯的物质的量与乙醇转化的物质的量的比值)随温度、乙烯进料量(单位: ![]() )的关系如图所示(保持其他条件相同)。
)的关系如图所示(保持其他条件相同)。
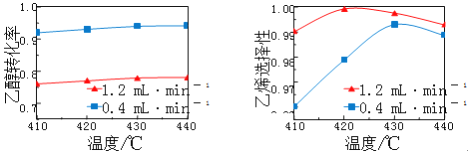
在410~440℃温度范围内,下列说法不正确的是
A. 当乙醇进料量一定,随乙醇转化率增大,乙烯选择性升高
B. 当乙醇进料量一定,随温度的升高,乙烯选择性不一定增大
C. 当温度一定,随乙醇进料量增大,乙醇转化率减小
D. 当温度一定,随乙醇进料量增大,乙烯选择性增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列转化关系中,A是一种日常生活中最常见的溶剂,G气体溶于水显碱性,Y 是胃酸的主要成分,K是不溶于稀硝酸的白色沉淀,反应⑤是工业制X的主要反应之一。1mol B通过反应②得到1mol F,B中F的质量分数为72%。
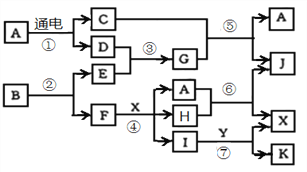
请按要求填空:
(1)B和G含有的共同元素在周期表中的位置是___________________。
(2)过量气体G与氯气反应可以生成一种单质和一种盐,该盐的电子式为 ________________________。
(3)写出反应④的离子方程式,并用单线桥标出电子转移情况__________________________。
(4)反应⑤的化学方程式为___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是中学常见的几种化合物,相关物质间的关系如下图所示(反应条件及部分产物均已略):
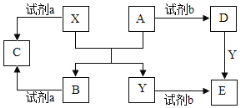
已知:X、Y是生活中常见的金属单质且X具有两性,A、B都是氧化物,A是红棕色粉末。回答下列问题:
(1)A的化学式为______________;
(2)若试剂b是稀硝酸。
①Y的单质与稀硝酸反应生成E时,Y单质必须过量,写出该反应的离子方程式__________________。如果稀硝酸过量,可以选择试剂________进行验证。
②D的阳离子能够与强碱、氯气反应,生成一种高效的净水剂YO42-,写出有关反应的离子方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中不是氧化还原反应的是
A. 3Cl2+6KOH===5KCl+KClO3+3H2O
B. CuO+H2![]() Cu+H2O
Cu+H2O
C. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
D. 2AgNO3+BaCl2===2AgCl↓+Ba(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料。已知A在标准状况下的密度为1.25 g·L-1,B可发生银镜反应。它们之间的转化关系如图:
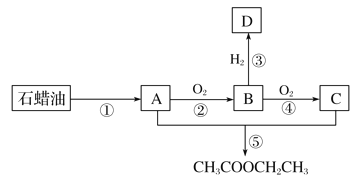
请回答:
(1)有机物B中含有的官能团名称是_______________________________________________。
(2)第⑤步发生加成反应,该反应的化学方程式是_________________________________。
(3)将金属钠与有机物D反应所得的少量产物溶于水,滴加2滴酚酞溶液,水溶液显红色,其原因是__________________(用化学方程式表示)。
(4)下列说法正确的是________。
A.有机物A与D在一定条件下可反应生成乙醚[(CH3CH2)2O]
B.用新制碱性氢氧化铜悬浊液无法区分有机物B、C和D
C.通过直接蒸馏乙酸乙酯和有机物C的混合物,可分离得到纯的乙酸乙酯
D.相同条件下乙酸乙酯在氢氧化钠溶液中水解较在稀硫酸中更完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )
A. Fe+CuSO4=FeSO4+Cu
B. 3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
C. AgNO3+NaCl=AgCl↓+NaNO3
D. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com