
| A.减少化石燃料的使用,开发新能源 |
| B.使用无氟冰箱,减少氟利昂排放 |
| C.多步行或乘公交车,少用私家车 |
| D.将工业废气用碱液吸收后再排放 |
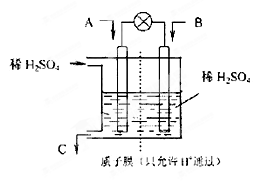
 n(H+)= mol。
n(H+)= mol。 N2O4(g) △H<0的平衡常数K=13.3。
N2O4(g) △H<0的平衡常数K=13.3。 CH3OH(g),己知该反应在300OC时的化学平衡常数为0.27,该温度下将2moI CO、3mol H2利2molCH3OH(g)充入容积为2 L的密闭容器中,此时反应将 。(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
CH3OH(g),己知该反应在300OC时的化学平衡常数为0.27,该温度下将2moI CO、3mol H2利2molCH3OH(g)充入容积为2 L的密闭容器中,此时反应将 。(填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。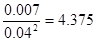 <13.3,这说明平衡向逆反应方向移动。应用反应是放热反应,所以是通过升高温度实现的。
<13.3,这说明平衡向逆反应方向移动。应用反应是放热反应,所以是通过升高温度实现的。 >0.27,所以反应是向逆反应方向移动的。
>0.27,所以反应是向逆反应方向移动的。

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源:不详 题型:填空题
| A.将硫酸厂搬离该镇 | B.建议环保部门限令整改 |
| C.将硫酸厂排出的废气中的SO2处理后排放 | D.工厂和居民改用较清洁的燃料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 污染物/g·km―1 | 速率/km·h-1 | ||
| 50 | 80 | 120 | |
| 一氧化碳 氮的氧化物 碳氢化合物 | 8.7 0.6 0.7 | 5.4 1.5 0.6 | 9.6 3.8 0.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.二氧化硫(SO2) | B.二氧化碳(CO2) |
| C.二氧化氮(NO2) | D.总悬浮颗粒物(TSP) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①与d | B.②与a | C.③与c | D.④与b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制CuSO4:Cu + 2H2SO4(浓) = CuSO4 + SO2↑+ 2H2O |
| B.制CuSO4:2Cu + O2△2CuO; CuO + H2SO4(稀) = CuSO4 + H2O |
| C.制Cu(NO3)2:Cu + 4HNO3(浓) = Cu(NO3)2 +2NO2↑+ 2H2O |
| D.制Cu(NO3)2:3Cu + 8HNO3(稀) = 3Cu(NO3)2 +2NO↑+ 4H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在化学反应中要考虑“原子经济性”以提高效率 |
| B.资源的开发和利用,要考虑可持续发展的原则 |
| C.要加强对工业“三废”的治理,以保护环境 |
| D.将废弃的塑料袋回收进行露天焚烧,以解决“白色污染”问题 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com