
| A. | 乙烯分子的比例模型示意图: | B. | 乙醇的分子式:CH3CH2OH | ||
| C. | 2-甲基-2-丁烯的键线式: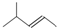 | D. | 硫化钠Na+[:$\underset{\stackrel{..}{S}}{..}$:]2Na+ |
分析 A.乙烯分子中含有4个碳氢键、1个碳碳键,所有原子共平面;
B.乙醇分子可以看作羟基取代了乙烷中的1个氢原子形成的,分子中存在1个甲基、1个亚甲基和1个羟基;
C.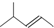 的主链为戊烯,名称为4-甲基-2-戊烯;
的主链为戊烯,名称为4-甲基-2-戊烯;
D.硫化钠为离子化合物,硫离子最外层满足8个电子的稳定结构.
解答 解:A.乙烯分子的结构简式为:CH2=CH2,比例模型能够体现出构成分子的各原子体积相对大小,乙烯的比例模型为: ,故A错误;
,故A错误;
B.乙醇分子中含有1个甲基、1个亚甲基和1个羟基,乙醇的结构简式为:CH3CH2OH,分子式为:C2H6O,故B错误;
C.2-甲基-2-丁烯,主链为丁烯,碳碳双键在2号C,而 的主链为戊烯,名称为4-甲基-2-戊烯,2-甲基-2-丁烯的结构简式为:CH3C (CH3)=CHCH3,其键线式为:
的主链为戊烯,名称为4-甲基-2-戊烯,2-甲基-2-丁烯的结构简式为:CH3C (CH3)=CHCH3,其键线式为: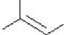 ,故C错误;
,故C错误;
D.硫化钠为离子化合物,硫离子最外层满足8个电子的稳定结构,电子式为:Na+[:$\underset{\stackrel{..}{S}}{..}$:]2Na+,故D正确,故选D.
点评 本题考查了球棍模型与比例模型、有机物键线式、电子式、分子式的判断,题目难度不大,注意掌握常见有机物结构与性质,明确球棍模型与比例模型的区别,试题培养了学生灵活应用所学知识的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 用如图所示的装置进行电解,在通电一段时间后,铁电极的质量增加.
用如图所示的装置进行电解,在通电一段时间后,铁电极的质量增加.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol C3H8(g)与5 mol O2(g)反应生成3 molCO2(g)和4 mol H2O(g)放出热量大于2220.0 kJ | |
| B. | 1 mol C3H6与4.5 mol O2反应生成3molCO2和3 mol H2O放出热量等于2049.0 kJ | |
| C. | 丙烷分子储存的能量大于丙烯分子 | |
| D. | 丙烷转化为丙烯的过程是一个吸热过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 .现有试剂:①Na; ②$\frac{{H}_{2}}{Ni}$;③Ag(NH3)2OH; ④新制Cu(OH)2; ⑤NaOH; ⑥KMnO4酸性溶液.
.现有试剂:①Na; ②$\frac{{H}_{2}}{Ni}$;③Ag(NH3)2OH; ④新制Cu(OH)2; ⑤NaOH; ⑥KMnO4酸性溶液.| A. | ①②⑤⑥ | B. | ①②④⑥ | C. | ①③④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,1 mol N2和3 mol H2充分反应,生成物中的N-H键数目为6NA | |
| B. | 完全燃烧1.5molCH3CH2OH和C2H4的混合物,转移电子数为18NA | |
| C. | 100 g 98%的浓硫酸中含氧原子个数为4NA | |
| D. | 1 L 0.1 mol/L的Na2S溶液中S2-和HS-的总数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Y>Z>R>T | |
| B. | 气态氢化物的稳定性:W<R<T | |
| C. | 最高价氧化物对应的水化物碱性:X>Y>Z | |
| D. | XR2、WR2两化合物中R的化合价相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如下转化关系:
A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如下转化关系:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com