
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ (””””)
A£®ŌŚŅ»¶ØĪĀ¶ČĻĀµÄAgClĖ®ČÜŅŗÖŠ£¬Ag£«ŗĶCl£ÅØ¶ČµÄ³Ė»żŹĒŅ»øö³£Źż
B£®AgClµÄKsp£½1.8”Į10£10 mol2·L£2£¬ŌŚČĪŗĪŗ¬AgCl¹ĢĢåµÄČÜŅŗÖŠ£¬[Ag£«]£½[Cl£]£¬ĒŅAg£«ŗĶCl£ÅØ¶ČµÄ³Ė»żµČÓŚ1.8”Į10£10mol2·L£2
C£®ĪĀ¶ČŅ»¶ØŹ±£¬ŌŚAgCl±„ŗĶČÜŅŗÖŠ£¬Ag£«ŗĶCl£ÅØ¶ČµÄ³Ė»żŹĒŅ»øö³£Źż
D£®Ļņ±„ŗĶAgClČÜŅŗÖŠ¼ÓČėŃĪĖį£¬Ksp±ä“ó
 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«aĘųĢåĶØČėBaCl2ČÜŅŗÖŠ£¬Ć»ÓŠ³ĮµķÉś³É£¬Č»ŗóŌŁĶØČėbĘųĢ壬ӊ³ĮµķÉś³É£¬Ōņa”¢b²»æÉÄÜŹĒ£Ø £©
A£®aŹĒCl2£¬bŹĒCO2 B£®aŹĒSO2£¬bŹĒCl2
C£®aŹĒNH3£¬bŹĒCO2 D£®aŹĒSO2£¬bŹĒCO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻÖÓŠČēĻĀĮ½øö·“Ó¦:
AӢNaOH + HCl = NaCl + H2O
BӢ2FeCl3+Cu =2FeCl2+CuCl2
£Ø1£©øł¾ŻĮ½·“Ó¦±¾ÖŹ, ÅŠ¶ĻÄÜ·ńÉč¼Ę³ÉŌµē³Ų£ŗA”¢_________£¬ B”¢__________
£ØŃ”Ōń”°ÄÜ”±»ņ”°²»ÄÜ”±£©£»
£Ø2£©Čē¹ū²»ÄÜ, ĖµĆ÷ĘäŌŅņ_______________________________________________
______________________________________________________________________£»
£Ø3£©Čē¹ūæÉŅŌ, ŌņŠ“³öÕż”¢øŗ¼«²ÄĮĻ¼°Ęäµē¼«·“Ó¦Ź½, µē½āÖŹČÜŅŗ£ŗ
øŗ¼«²ÄĮĻ________£¬µē¼«·“Ó¦Ź½_______________£¬µē½āÖŹČÜŅŗ____________£»
Õż¼«²ÄĮĻ________£¬µē¼«·“Ó¦Ź½_______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
øł¾Ż³ĀŹöµÄÖŖŹ¶£¬ĄąĶĘµĆ³öµÄ½įĀŪÕżČ·µÄŹĒ
A£®Ć¾ĢõŌŚæÕĘųÖŠČ¼ÉÕÉś³ÉµÄŃõ»ÆĪļŹĒMgO£¬ŌņÄĘŌŚæÕĘųÖŠČ¼ÉÕÉś³ÉµÄŃõ»ÆĪļŹĒNa2O
B£®ŅŃÖŖ¢ōA·ŠµćCH4£¼SiH4£¼GeH4£¬Ōņ¢õA×å·Šµć NH3£¼PH3£¼AsH3
C£®ŅŃÖŖFeÓėSÖ±½Ó»ÆŗĻÉś³ÉFeS£¬ŌņCuÓėSÖ±½Ó»ÆŗĻÉś³ÉCu2S
D£®ŅŃÖŖCa(HCO3)2 +2NaOH(¹żĮæ) £½ CaCO3”ż+ Na2CO3+ 2H2O£¬Ōņ
Mg (HCO3)2 +2NaOH(¹żĮæ) £½ MgCO3”ż+ Na2CO3+ 2H2O
(HCO3)2 +2NaOH(¹żĮæ) £½ MgCO3”ż+ Na2CO3+ 2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®ÓÉŅ»ÖÖŌŖĖŲ×é³ÉµÄĪļÖŹæÉÄÜŹĒ»ģŗĻĪļ
B£®Ķ¬Ņ»Ö÷×å²»Ķ¬ŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ£¬¾§Ģå½į¹¹Ņ»¶ØĻąĶ¬
C£®×īĶā²ćµē×ÓŹżĪŖ1µÄŌŖĖŲŅ»¶ØŹĒÖ÷×åŌŖĖŲ
D£®ÓÉ·Ē½šŹōŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļŅ»¶ØŹĒ¹²¼Ū»ÆŗĻĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀĻĀ£¬ĻĀĮŠĄė×ÓÅØ¶ČµÄ¹ŲĻµÕżČ·µÄŹĒ (””””)
A£®pH£½2µÄŃĪĖįÓėpH£½12µÄ°±Ė®µČĢå»ż»ģŗĻ£ŗ
c(NH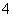 )£½c(Cl£)£¾c(H£«)£½c(OH£)
)£½c(Cl£)£¾c(H£«)£½c(OH£)
B£®0.2 mol·L£1µÄCH3COONaČÜŅŗÓė0.1 mol·L£1µÄHClµČĢå»ż»ģŗĻ£ŗ
c(Na£«)£¾c(Cl£)£¾c(CH3COO£)£¾c(H£«)£¾c(OH£)
C£®0.1 mol·L£1µÄHCN(ČõĖį)ŗĶ0.1 mol·L£1µÄNaCNµČĢå»ż»ģŗĻ£ŗ
c(HCN)£«c(CN£)£«c(OH£)£½c(Na£«)£«c(H£«)
D£®ĻąĶ¬ĪļÖŹµÄĮæÅØ¶ČŹ±£¬ČÜŅŗÖŠc(NH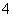 )Óɓ󵽊”µÄĖ³Šņ£ŗNH4Al(SO4)2£¾NH4Cl£¾CH3COONH4£¾NH3·H2O
)Óɓ󵽊”µÄĖ³Šņ£ŗNH4Al(SO4)2£¾NH4Cl£¾CH3COONH4£¾NH3·H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀĻĀ£¬ÓŠĻĀĮŠ4ÖÖČÜŅŗ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ (””””)
| ¢Ł | ¢Ś | ¢Ū | ¢Ü |
| 0.1 mol·L£1 CH3COOHČÜŅŗ | pH£½3 CH3COOHČÜŅŗ | 0.1 mol ·L£1 NaOHČÜŅŗ | pH£½11 NaOHČÜŅŗ |
A.ÓÉĖ®µēĄė³öµÄc(H£«)£ŗ¢Ū£¾¢Ł
B£®¢ŁĻ”ŹĶµ½ŌĄ“µÄ100±¶ŗó£¬pHÓė¢ŚĻąĶ¬
C£®¢ŁÓė¢Ū»ģŗĻ£¬ČōČÜŅŗpH£½7£¬ŌņĮ½ÖÖČÜŅŗµÄĢå»ż£ŗ¢Ū£¾¢Ł
D£®¢ŚÓė¢Ü»ģŗĻ£¬ČōČÜŅŗpH£½7£¬ŌņĮ½ÖÖČÜŅŗµÄĢå»ż£ŗ¢Ü£¾¢Ś
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«2mol SO2ŗĶ2mol SO3ĘųĢå»ģŗĻÓŚ¹Ģ¶ØČŻ»żµÄČŻĘ÷ÄŚ,ŌŚŅ»¶ØĢõ¼žĻĀ,·¢Éś·“Ó¦:
2SO2 + O2 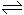 2SO3,“ļĘ½ŗāŹ±SO3ĪŖn mol”£ĻąĶ¬ĪĀ¶ČĻĀ·Ö±š°“ĻĀĮŠÅä±Č,Ę½ŗāŗóSO3µÄĪļÖŹµÄĮæ“óÓŚn molµÄŹĒ
2SO3,“ļĘ½ŗāŹ±SO3ĪŖn mol”£ĻąĶ¬ĪĀ¶ČĻĀ·Ö±š°“ĻĀĮŠÅä±Č,Ę½ŗāŗóSO3µÄĪļÖŹµÄĮæ“óÓŚn molµÄŹĒ
A£®2mol SO2ŗĶ1mol O2 B£®2mol SO2ŗĶ1mol O2ŗĶ2mol SO3
C£®4mol SO2ŗĶ1mol O2 D£®3mol SO2ŗĶ0.5mol O2ŗĶ1mol SO3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÖŹĮ涼ŹĒ50 gµÄHCl”¢NH3”¢CO2”¢O2ĖÄÖÖĘųĢå£ŗ
(1)ŗ¬ÓŠ·Ö×ÓŹżÄæ×īÉŁµÄŹĒ________£»
(2)Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬Ģå»ż×ī“óµÄŹĒ________£»ĆܶČ×īŠ”µÄŹĒ________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com