
下列离子方程式书写正确的是
A.稀硝酸溶液中加入氢氧化亚铁:Fe(OH)2+2H+=Fe2++2H2O
B.NaOH溶液中加入过量Ba(HCO3)2溶液:Ba2++2OH-+2HCO3-=BaCO3↓+2H2O+CO32-
C.FeI2溶液中通入极少量Cl2:2I-+Cl2=I2+2Cl-
D.AICl3溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O
科目:高中化学 来源:2015-2016学年江西省南昌市高一上学期期中测试化学试卷(解析版) 题型:填空题
(1)下列物质能导电的是 ,属于电解质的是 ,
属于非电解质的是 。
①NaCl晶体 ②液态SO2 ③液态醋酸 ④汞 ⑤BaSO4固体
⑥纯蔗糖(C12H22O11) ⑦氨水 ⑧熔化的KNO3
(2)按要求写出下列方程式:
①KHSO4熔融状态电离方程式:_________________
②苏打与过量稀盐酸反应的离子方程式:_________________
(3)①36g水中氧原子的物质的量为: _________________。
②在同温同压下,相同体积的O2和CH4,原子数目之比为______________。
③含有6.02×1023个氦原子的氦气在标准状况下的体积约为 。
查看答案和解析>>
科目:高中化学 来源:2016届广西省钦州市钦南区高三上学期期中质量调研测试化学试卷(解析版) 题型:选择题
Zn(OH)2是两性氢氧化物,和强酸反应时生成Zn2+,跟强碱反应时生成ZnO22-.现有三份等物质的量浓度、等体积的MgCl2、ZnCl2、AlCl3溶液(配制时均加入少量盐酸),现将一定浓度的NaOH溶液,分别滴入三种溶液中至过量,NaOH溶液的体积x(mL)与生成沉淀的物质的量y(mol)的关系如下图所示,则与MgCl2、ZnCl2、AlCl3三种溶液一一对应的正确图象是

A.③②① B.③②④ C.③⑤① D.③⑤④
查看答案和解析>>
科目:高中化学 来源:2016届河南省南阳市高三上学期期中质量评估化学试卷(解析版) 题型:实验题
用纯碱和双氧水混合可制作新型液体洗涤剂(2Na2CO3·3H2O2),它具有杀菌消毒去油污的能力且不会污染水源。
(1)检验这种新型洗涤剂中金属阳离子的操作和现象是 。
(2)这种洗涤剂中的双氧水可以将废水中的CN一转化生成NH3,写出该反应的离子方程式 。
(3)如果配制洗涤剂的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至会完全失去杀菌作用。试分析其中可能的原因(写出其中一种即可,用离子方程式和简要文字表述)____________________。
(4)某化学学习小组为了定性探究铁离子对这种新型洗涤剂的不良影响,取该洗涤100mL,加入25gFeCl3固体,产生大量无色无味气体,用贮气瓶收集气体。请选用下列试剂和实验用品完成气体成分的探究过程:0.10mol.L-l NaOH溶液、8.0mol.L-l NaOH:溶液、澄清石灰水、0.l0mol.L-1 KMn04溶液、BaCI2稀溶液、品红溶液、蒸馏水、木条、酒精灯、火柴、洗气瓶。
①提出假设:对该气体成分提出合理假设。
假设1:气体是O2。
假设2:气体是CO2。
假设3:气体是
②设计方案:设计实验方案证明你的假设,在下表中完成实验步骤、预期现象和结论。
实验步骤 | 预期现象和结论 |
将气体依次通入盛有_____________________、________________的洗气瓶中,并_______________。 | ___________________________________ |
查看答案和解析>>
科目:高中化学 来源:2016届河南省南阳市高三上学期期中质量评估化学试卷(解析版) 题型:选择题
铁粉和铜粉的均匀混合物,平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只和NO):下列计算结果错误的是
编号 | ① | ② | ③ | ④ |
稀硝酸体积/mL | 100 | 200 | 300 | 400 |
剩余金属/g | 18.0 | 9.6 | 0 | 0 |
NO体积/mL | 2240 | 4480 | 6720 | V |
A.①中溶解了8.4gFe
B.原混合物总质量为105.6g
C.硝酸的浓度为4mol/L
D.④中V=6720
查看答案和解析>>
科目:高中化学 来源:2016届湖北省松滋市高三上学期期中测试化学试卷(解析版) 题型:填空题
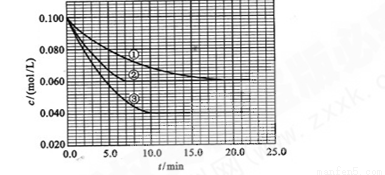
在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100 kJ·mol-1、c(B)=0.200 kJ·mol-1及c(C)=0 kJ·mol-1。反应物A的浓度随时间的变化如下图所示。
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100 kJ·mol-1、c(B)=0.200 kJ·mol-1及c(C)=0 kJ·mol-1。反应物A的浓度随时间的变化如下图所示。
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件;所改变的条件分别:
②_______________;③_______________。
(2)实验②平衡时B的转化率为_________;该反应的△H _____0;(填“>”、“<”、或“=”)理由是_________________________________________。
(3)该反应进行到4.0min时的平均反应速率:实验③:v(B)=___________________。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省松滋市高三上学期期中测试化学试卷(解析版) 题型:选择题
X、Y均为元素周期表ⅦA族中的两种元素。下列叙述中,能够说明X的原子得电子能力比Y强的是
A.原子的电子层数:X>Y
B.对应的简单离子的还原性:X>Y
C.气态氢化物的稳定性:X>Y
D.氧化物对应水化物的酸性:X>Y
查看答案和解析>>
科目:高中化学 来源:2016届江苏省南通市高三上学期第一次阶段测化学试卷(解析版) 题型:实验题
硼镁矿属于硼酸盐,可用来制备硼酸(H3BO3)和MgO,方法如下:硼镁矿粉与(NH4)2SO4溶液混合后加热,反应生成H3BO3晶体和MgSO4溶液,同时放出NH3;再向MgSO4溶液中通入NH3与CO2,得到MgCO3沉淀和滤液,沉淀经洗涤、煅烧后得MgO,滤液则循环使用。回答下列问题:
(1)与硅酸盐类似,硼酸盐结构也比较复杂,如硬硼钙石化学式为Ca2B6O11·5H2O,将其改写为氧化物的形式 。
(2)上述制备过程中,检验沉淀洗涤是否完全的方法是 。
(3)写出MgSO4溶液中通入NH3与CO2反应的化学方程式 。
(4)若准确称取1.68 g硼镁矿,完全反应后得H3BO3晶体1.24 g,MgO 0.8 g,计算该硼酸盐的组成。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一上学期10月月考化学试卷(解析版) 题型:填空题
实验题:现需要90 mL 1.00 mol·L-1 NaCl溶液,某同学按下列步骤进行配制:
①计算所需NaCl固体的质量;
②称量NaCl固体;
③将称好的NaCl固体放入烧杯中,用适量蒸馏水溶解;
④将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶;
⑤向容量瓶中加蒸馏水至刻度线。
请回答有关问题:
(1)计算所需NaCl固体的质量______g。
(2)为了加速溶解,可以采取的措施是_______________。
(3)使用容量瓶的规格是________mL。
(4)如果将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外,最后配成的溶液中溶质的实际浓度比所要求______________(填“大”或“小”)了。
(5)如果某同学是用托盘天平称量NaCl固体,那么称量的质量是 ,与计算量一致吗?解释原因___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com