
分析 (1)在蒸发结晶的过程中,还需进行的手动操作是搅拌,防止液体飞溅,当有较多晶体析出时即停止加热;
(2)加入氯化钡溶液检验硫酸根离子是否除尽;
(3)在粗盐提纯的过程中需要滴加饱和Na2CO3溶液除去钙离子以及过量的钡离子.
解答 解:(1)在蒸发结晶的过程中,为了防止液体飞溅,还需进行的手动操作是搅拌;当蒸发皿中有较多晶体析出时即停止加热,利用余热将剩余液体蒸干,
故答案为:用玻璃棒搅拌,防止液体飞溅;蒸发皿中产生了较多的固体;
(2)加入过量氯化钡溶液除去硫酸根离子,检验硫酸根离子已除尽,可静止片刻在上层清液处,滴加一滴氯化钡溶液,不出现浑浊就说明硫酸根离子已经除尽,如果还有,可以在溶液中继续加入过量的氯化钡,
故答案为:静置片刻后,取上层清液于试管中,继续滴加氯化钡,若出现浑浊或白色沉淀,说明溶液中含有硫酸根,否则不含硫酸根;在溶液中继续加入过量的氯化钡;
(3)碳酸钠与镁离子生成碳酸镁沉淀、与钙离子生成碳酸钙沉淀、与钡离子生成碳酸钡沉淀,所以滴加饱和碳酸钠溶液,可以除去钙离子、镁离子和过量的钡离子,
故答案为:除去Ca2+、Mg2+及加入过量的Ba2+.
点评 本题考查在粗盐提纯的过程中所选用除杂和净化的方法,题目难度不大,注意除去杂质不要引入新的杂质,对于实验过程中过量的试剂都要除去.


科目:高中化学 来源: 题型:选择题
| A. | 不能确定HCO3-离子是否存在 | B. | 可能有CO32-离子 | ||
| C. | 一定有Cl-离子存在 | D. | 一定有SO42-离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| J | ||||
| R |
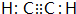 .
.| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入氧气 | 加入乙的物质 |
| y | 乙的物质的量 | 平衡常数K | 乙的转化率 | 生成物物质的量总和 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
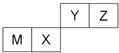
| A. | 原子半径Z<M | |
| B. | Z位于元素周期表中第2周期、第ⅥA族 | |
| C. | X的最简单气态氢化物的热稳定性比Z的小 | |
| D. | X的最高价氧化物不溶于任何酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀. |
| 实验步骤 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) | C | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:3 | B. | 1:3 | C. | 1:1 | D. | 1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com